
# 热门搜索 #
罕见病基因治疗市场走热,诺华、辉瑞、蓝鸟、 Spark、博雅辑因……16家基因治疗公司如何布局?
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持本文摘选自探针资本《罕见病基因治疗行业研究》报告
罕见病研究是基因治疗的重点应用领域,后者被认为是最有可能从根本上治愈罕见病的解决方案。但从目前各大公司的研发管线来看,研究方向仍然集中于某几种单基因遗传病或部分病因较为明确的多基因疾病上。这一数量相比于全球已经发现的罕见病种类而言仍然非常有限。其中的限制因素不仅包括科研中相关病因尚未完全揭示,同时也包括传统基因递送的治疗方式中,基因递送载体的容量限制和免疫原性、新型基因编辑技术本身还并未被广泛验证的脱靶效应、同源重组效率等因素。因此,随着科研的进步,使用新型基因治疗技术(编辑工具、治疗基因的改造)+新型/不断优化的基因递送载体的组合治疗,罕见病将会有非常广泛的应用前景。
EvaluatePharma于今年初发布报告,预计在未来六年内,将有大约60种基因疗法产品获批。这些药物的销售额在2024年将达到146亿美元,约占全球医药总收入的1.2%。即使罕见病基因疗法目前存在适应症有限、价格高昂以及可及性等诸多问题,这一全新疗法相关技术在其他治疗领域的可扩展性、疗效预期以及世界各国政府监管机构的支持都使之受到了广泛的关注,同时其未来的巨大市场也吸引了众多的投资。
根据动脉网知识库统计,2018年全球共有20家基因治疗企业获得融资,融资总额17亿美元。2019年上半年,基因治疗领域共有13家医药企业获得融资,融资总额12亿美元。此外,越来越多的大型制药公司,如诺华、百健、罗氏、辉瑞以及赛默飞、CRO公司等也正在通过并购、或与基因疗法药企深度合作的方式扩大或引入自身在基因治疗的业务板块,通过掌握核心技术以及生产能力保证在这一赛道的竞争力。
按照不同公司核心技术的情况,可将基因治疗公司大致分为以rAAV/慢病毒递送系统为核心的基因递送公司和以基因编辑技术为核心的基因编辑公司。目前该领域国外代表性公司大多已实现上市或被收购,同时还有一大批公司处于不同轮次的融资阶段;国内由于起步较晚,相关公司数量较少,且处于比较早期的融资阶段。领域内国内外公司的融资/并购/上市情况如下表所示。
罕见病基因治疗领域代表性公司简介
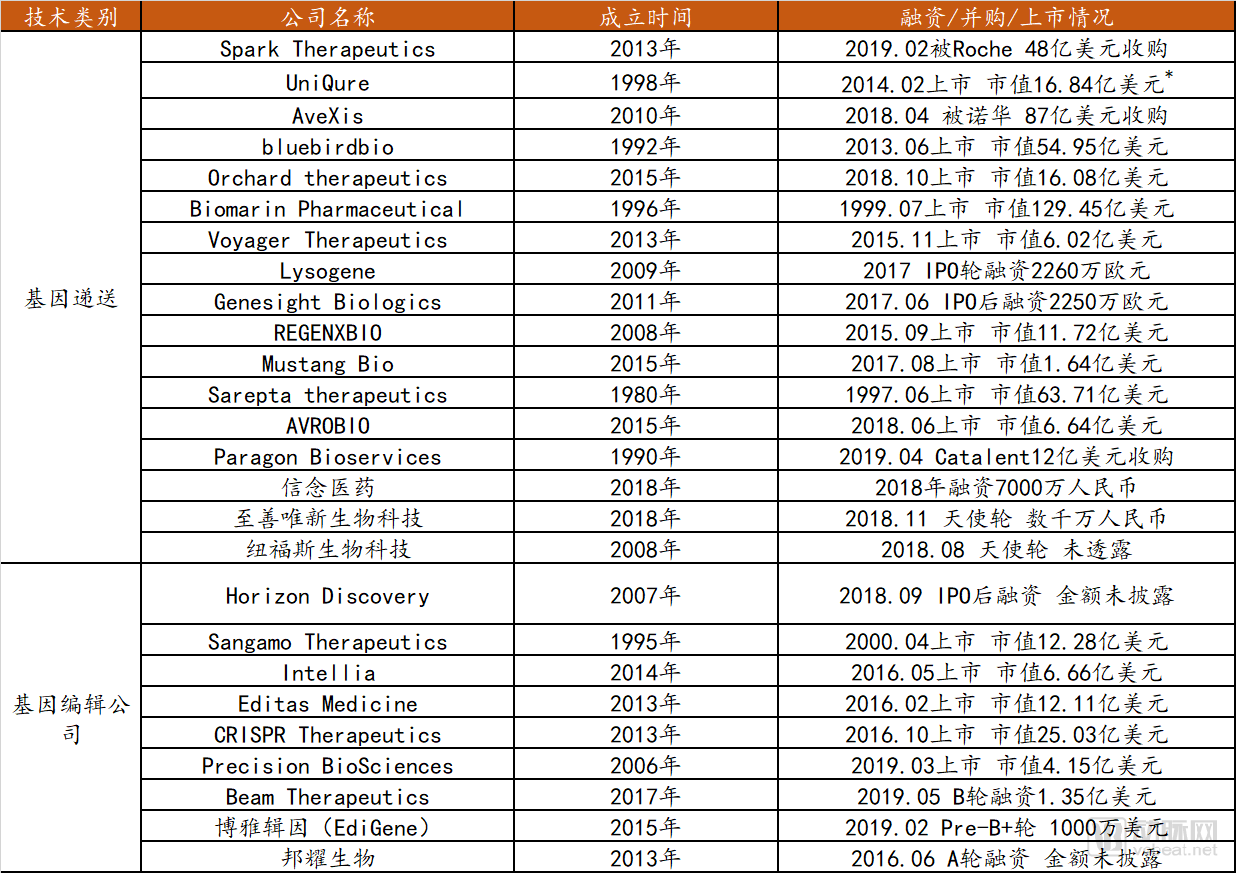
来源:公开资料整理
基因递送公司
诺华近两年通过合作和并购的方式不断扩大公司在基因治疗领域的布局。2018年1月,诺华与Spark Therapeutics签订了许可和供应协议,获得了FDA 2017年批准上市用于治疗先天性黑朦的药物Luxturna在美国以外市场的开发、注册和商业化权利。2018年4月,诺华以87亿美元的价格将AveXis收购。
AveXis公司创立于2010年,总部位于伊利诺伊州,于2016年2月在纳斯达克上市,核心技术是以AAV9为载体进行的基因治疗,致力于开发针对脊髓性肌萎缩(SMA)的新型基因疗法。该公司的主打产品Zolgensma在2019年5月获美国FDA批准。因此,诺华对AveXis的收购使之拥有了针对脊髓性肌萎缩症(SMA)儿童患者的首个且唯一基因疗法。
AveXis融资信息
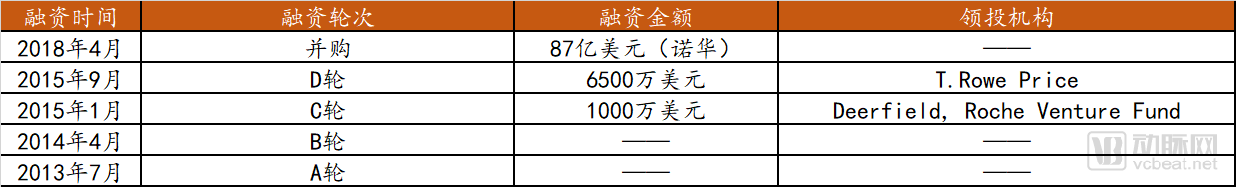
数据来源:crunchbase
2018年5月,诺华公布一系列政策,剥离了部分业务,将重点放在变革药物上,专注于细胞及基因治疗。2018年8月,欧盟批准诺华CAR-T细胞疗法;2018年11月,欧盟批准诺华的Luxturna。截至目前,诺华拥有全球获批细胞/基因疗法中的半数产品,成为再生医学领域当之无愧的巨头。公司管线中的听力药CGF166和治疗视网膜色素病变的CPK850现已进入临床试验。

图17.诺华基因治疗研发产品管线(来源:公司官网)
Spark Therapeutics成立于2013年,是一家基因治疗公司,于2015年在纳斯达克上市。2019年2月,罗氏以48亿美元收购Spark Therapeutics,并计划对spark therapeutics产品组合进行投资。Spark Therapeutics将在罗氏集团的架构下继续以独立公司进行运营。
Spark Therapeutics融资信息
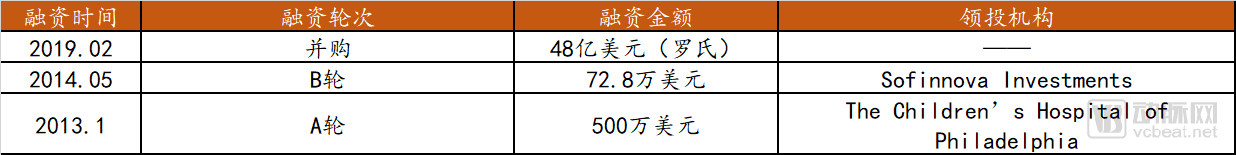
数据来源:crunchbase
Spark首席执行官Jeffrey Marrazzo具有多年遗传病治疗领域研发经验,公司的核心技术是AAV的基因治疗,针对遗传性视网膜病变(inherited retinal diseases IRDs)、神经退行性病变、血液系统疾病进行药物研发。公司有320多名领域内的专业员工,在菲律宾有48000立方英尺的全球最先进的cGMP工厂生产AAV载体,有6条线路来满足超过12个临床试验中心的临床试验进行,最后组装成药物来满足临床需要。
2017年12月视网膜萎缩症药物Luxturna获美国FDA批准上市,这也是首款一次性基因治疗RPE65等位基因突变的药物。2018年11月,通过与诺华合作,Luxturna也获得了欧盟的批准。
目前Spark研发管线中速度最快的两个药物是针对B型和A型血友病的三期临床试验,其中针对B型血友病的SPK-9001疗法已获得FDA授予的孤儿药和突破性药物资格,欧洲药品管理局EMA也为其颁发了PRIME认定。
2018年7月,Spark公司达成了与辉瑞的协议,使得SPK-9001的临床Ⅲ期以及后续监管、生产及全球商业化均由辉瑞承担。A型血友病的发病率是B型的4倍,因而具有更加广阔的市场。针对A型血友病的SPK-8011于2018年底启动Ⅲ期临床试验,如果这一基因疗法成功,将帮助罗氏扩大其在A型血友病领域的影响力,进而与武田制药、赛诺菲等形成竞争。
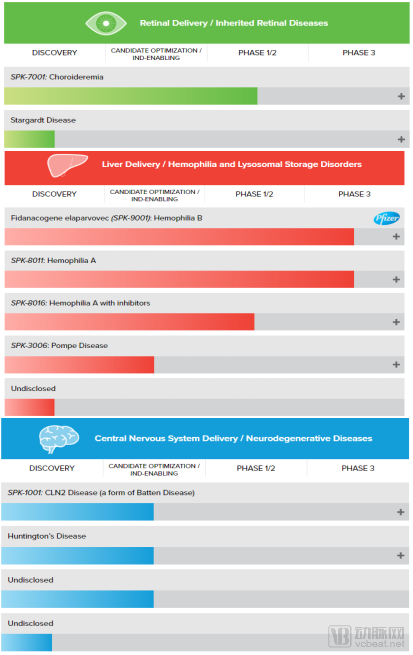
Spark Therapeutics公司研发产线(来源:公司官网)
Nightstar Therapeutics创立于2013年,总部位于英国,是一家基因治疗方法研发商,专注于用AAV治疗遗传性视网膜疾病研究,于2018年在纳斯达克上市。2019年,其全部股份被百健Biogen以8.77亿美元收购。
Nightstar Therapeutics融资信息
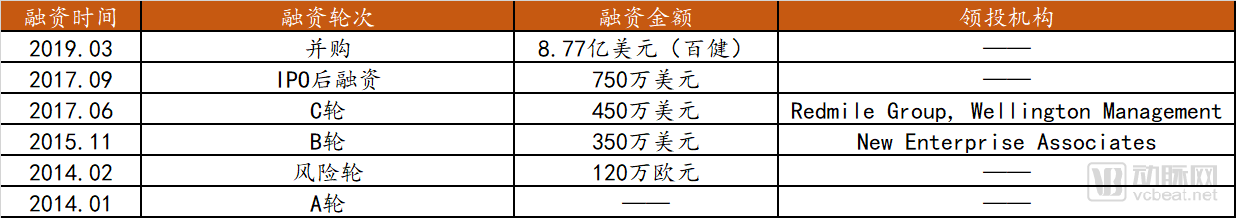
数据来源:crunchbase
目前公司推出了两款治疗视网膜疾病的基因疗法。主要产品 NSR-REP1正处于Ⅲ期临床阶段,针对无脉络膜症(一种罕见的视网膜疾病,目前尚无医治手段)。另一款NSR-RPGR针对色素性视网膜炎(XLRP)正处于1/2期临床试验阶段。此外,Nightstar还拥有丰富的临床前候选管线,包括针对Stargardt (一种常染色体隐性遗传疾病,与ABCA4基因突变有关)的NSR-ABCA4及针对Best卵黄样黄斑营养不良的NSR-BEST1。
在无脉络膜症的市场竞争中,Nightstar Therapeutics的最强竞争对手Spark Therapeutics。但其相关管线仍处于临床Ⅰ/Ⅱ期试验阶段,目前看来Nightstar处于较为有利的地位。随着这两家公司接连被Biogen和Roche收购,该治疗领域已变成了Roche和Biogen两家制药巨头之间的竞争。
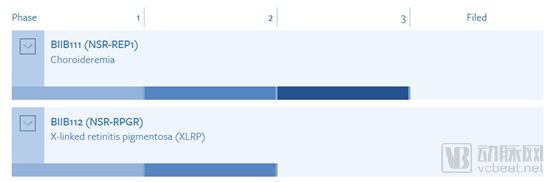
Nightstar Therapeutics基因治疗相关管线(来源:公司官网)
辉瑞制药近5年来在基因治疗领域的一系列收购与合作证明了公司希望成为基因治疗领域领头羊的决心。
早在2014年,辉瑞就与Spark Therapeutics达成战略协议,共同开发B型血友病基因疗法SPK-9001。2017年起,辉瑞与ZFN技术巨头Sangamo针对A型血友病基因疗法签署了高达4.75亿美元潜在里程碑付款的协议,其中3亿美元为SB-525开发和商业化相关的里程碑金,其余1.75亿美元为其他A型血液病基因疗法的里程碑金。此外,辉瑞还将支付此次合作所诞生产品在未来销售额达2位数的特许权使用费。
2018年,辉瑞与Sangamo二度合作,收购了其旗下治疗肌萎缩性脊髓侧索硬化症(ALS)的基因疗法。2019年3月,辉瑞斥资6.36亿美元收购法国Vivet Therapeutics公司15%的股份,共同开发一款基于新型改造的AAV载体,针对威尔逊病(WD)的基因疗法VTX-801V。
2019年辉瑞与拥有100多种新型AAV载体技术平台的REGENXBIO公司达成研发许可协议。辉瑞可以使用REGENXBIO公司专有的AAV9载体开发基因疗法,用于治疗弗里德莱西共济失调(Fredreich’s ataxia, FA)。该疾病发病率约为1/5万,患者表现为失去协调和平衡能力、肌肉无力、视力受损、实力和语言障碍、脊柱侧凸、糖尿病和心肌病等一系列并发症。同月,辉瑞宣布了一项5亿美元的计划用于在北卡桑德福扩建基因治疗生产设施,加强公司在制造高度专业化、使用定制的rAAV载体以支持其基因治疗研究和开发的能力。
Voyager Therapeutics成立于2013年,总部位于剑桥,华人学者高广坪博士是联合创始人之一。公司于2015年在纳斯达克上市,2019年2月,获得由Neurocrine制药公司的6500万美元战略投资。
Voyager Therapeutics融资历史
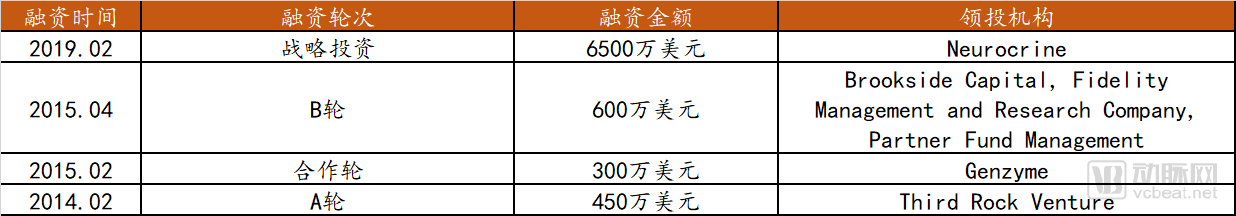
数据来源:crunchbase
Voyager的核心技术是AAV基因治疗,在载体优化工程、给药技术以及工艺开发和生产方面均有创新,专注于为患有严重神经系统疾病的患者开发治疗方法。
Voyager主打产品为VY-AADC,可以将AADC基因直接递送至多巴胺受体所在的壳核神经元中,绕过黑质神经元,使壳核中的神经元表达 AADC 酶,将左旋多巴转化为多巴胺。目前Voyager向FDA提交的帕金森病创新疗法VY-AADC的Ⅱ和Ⅲ期关键临床试验计划得到了认可。如果Ⅱ期试验结果积极,VY-AADC可直接递交上市申请,预计其Ⅱ期临床实验将于2020年底完成,其他临床前研究见下图。
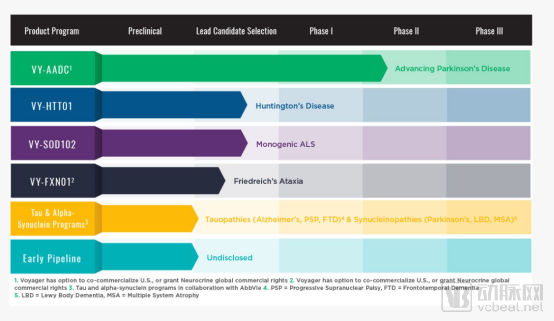
Voyager Therapeutics公司研发管线(来源:公司官网)
2018年,Voyager与艾伯维达成合作,通过AAV载体的基因疗法,治疗阿尔兹海默症等神经退行性疾病。2019年初,又与艾伯维达成协议,重点关注帕金森病基因治疗。此外,该公司与赛诺菲 Genzym、马萨诸塞大学和MRI Interventions签有战略合作协议。
蓝鸟生物创立于1992年,前称Genetix Pharmaceuticals, Inc.于2010年9月改为现用名。公司总部位于美国马萨诸塞州剑桥市,全职雇员479人,是一家临床阶段的生物技术公司,与2013年在纳斯达克上市。蓝鸟生物致力于为治疗严重的遗传疾病和罕见疾病开发革命性基因疗法,公司核心技术是慢病毒基因治疗。
蓝鸟生物融资情况
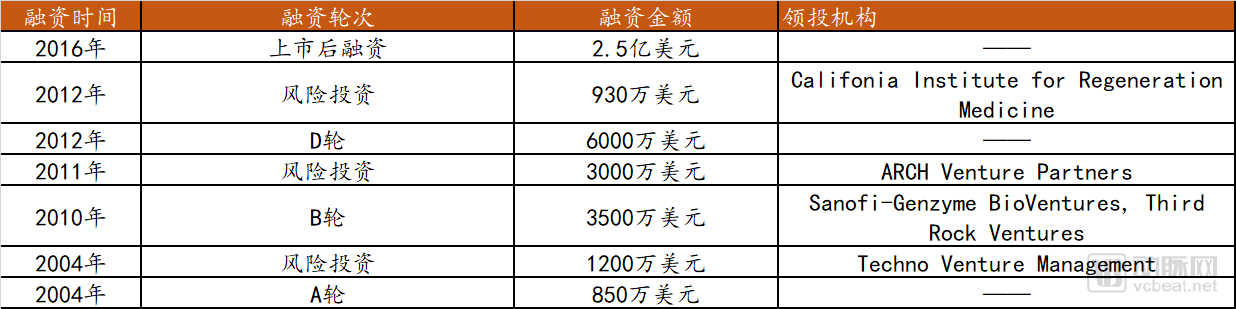
数据来源:crunchbase
2019年6月, Bluebird Bio公司宣布欧盟委员会(EC)有条件批准其基因疗法Zynteglo(以前称为LentiGlobin™)上市,治疗12岁及以上患者的输血依赖型β地中海贫血。Zynteglo是针对这一疾病的全球首款基因疗法。
除上述的Zynteglo,公司研发管线中速度最快的还有Lenti-D,这款基因疗法将正常的ABCD1基因转入到了患者自身的干细胞内,协助产生具有正常功能的ALDP酶。这些酶能有效地降解超长链脂肪酸,抑制由CALD带来的神经退行症状,来治疗脑肾上腺脑白质营养不良。2018年5月,美国FDA已授予其突破性疗法认定。
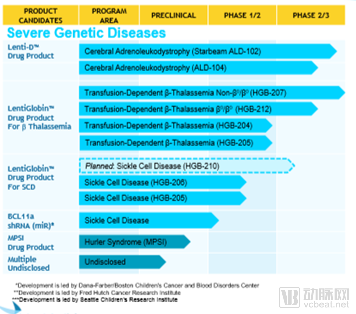
蓝鸟生物基因疗法研发管线(来源:公司官网)
Uniqure成立于1998年,总部设在荷兰。2014年公司在纳斯达克正式上市,它核心技术是基于AAV的基因治疗,在AAV5用于递送至脑或肝的治疗产品中拥有独家的全球权利,公司主要从事罕见病领域的基因治疗。
Uniqure融资历史

数据来源:Crunchbase
该公司的第一个产品是Glybera,用于脂蛋白脂酶缺乏症(LPLD)的治疗。该产品于2012年10月,获得欧盟药物管理机构批准,但上市后受到高昂的价格和小众市场的影响,该药物现已退市。目前公司的产品围绕血友病、亨廷顿舞蹈症以及其他疾病。AMT-061是其在血友病和亨廷顿氏病的候选产品,使用载体的AAV5变体或血清型为载体,用于治疗B型血友病,目前正在进行Ⅱ/Ⅲ临床试验;另一产品AMT-130,利用公司专有的miQURETM沉默技术,其载体为携带人工微RNA(micro-RNA, miRNA)的AAV5载体,该载体专门用于沉默亨廷顿基因,用于治疗亨廷顿病。FDA于2019年1月批准其IND。
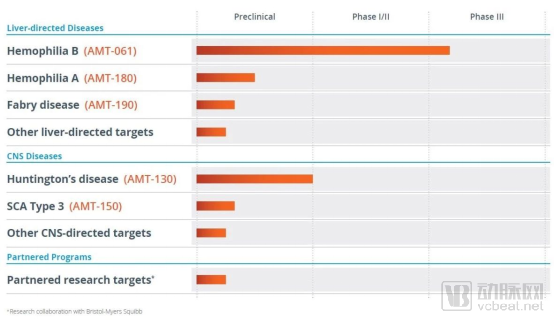
Uniqure公司研发管线(来源:公司官网)
BioMarin成立于1996年,总部位于美国加州,于1999年在纳斯达克上市。BioMarin是一家全球性的制药公司,其核心技术是AAV基因治疗,专注于为患有危重的罕见的遗传病患者提供医疗帮助。
公司已上市的产品涵盖多种罕见遗传疾病的替代疗法,主要有治疗Morquio A综合征的Vimizim®、治疗肌无力综合征的Firdapse®、针对粘多糖贮积症VI(MPS VI)的Naglazyme®、用于苯丙酮尿症(PKU)的Kuvan®及用于粘多糖贮积症I(MPS I)的Aldurazyme®。
在基因治疗领域,目前主打产品是Valoctocogene Roxaparvovec(BMN 270),用于治疗A型血友病,正在进行Ⅲ期临床试验。Valoctocogene Roxaparvovec利用AAV5向患者体内递送人凝血因子Ⅷ功能基因,恢复人凝血因子Ⅷ的正常分泌。公司计划于2019年第四季度向美国FDA和欧洲EMA提交加速批准申请,该产品预计将成为首款进入监管审评阶段的血友病基因疗法。2018年5月,BioMarin治疗苯丙酮尿症(PKU)的酶替代疗法在FDA获批,在该治疗领域,公司的一种基因疗法BMN 307目前正处于临床前测试,计划在2019年下半年提交IND。
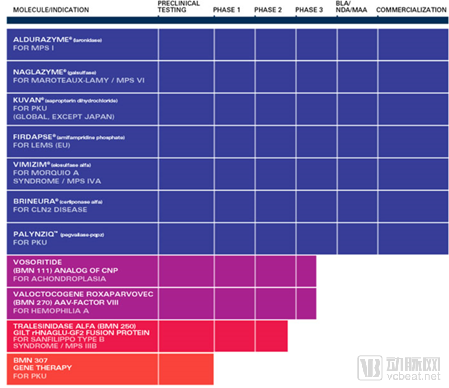
BioMarin公司研发管线 (来源:公司官网)
Orchard Therapeutics创立于2015年,是英国的一家生物技术公司,在美国洛杉矶设有办事处。公司于2018年在纳斯达克上市。
Orchard Therapeutics融资历史
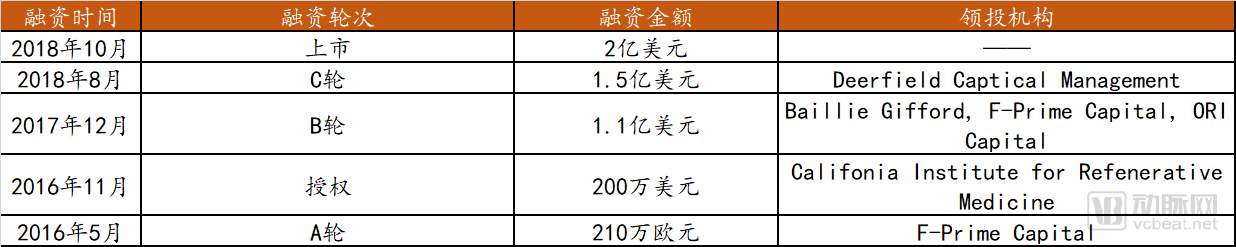
数据来源:Crunchbase
Orchard专注于罕见疾病,聚焦于自体造血干细胞基因疗法上,核心技术是离体自体细胞干细胞基因治疗和慢病毒载体。2018年,Orchard公司以19.9%的股份做交换,收购了GSK的罕见疾病基因治疗产品(包括OTL-200和OTL -103),囊括了已经EMA批准上市的体外基因治疗药物Strimvelis。目前公司管线包括对三类罕见病的药物研发:
1.输血依赖性β地中海贫血(TDBT),该药物在2018年已被EMA授予优先药物资格;
2.原发性免疫缺陷疾病,包括ADA-SCID, WAS以及X-CGD;
3.遗传性代谢疾病,如黏液多糖贮积症ⅢA型 (MPS-ⅢA)和ⅢB型 (MPS-ⅢB)的项目。针对MPS-ⅢA的OTL-201已进入临床试验阶段,同时OTL-102,OTL-300也已经处于临床试验接近完成的状态。
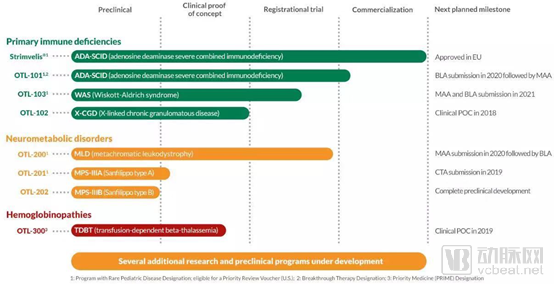
Orchard Therapeutics公司产品研发管线(来源:公司官网)
因其女儿被诊断出患有罕见的神经退行性疾病,Karen Aiach在2009年创立Lysogene,公司在2014年完成A轮融资220万美元。2017年,在巴黎证券交易所的一次小型首次公开募股的帮助下,该公司为其GM1神经节苷脂病的基因疗法进行了募资。
Lysogene融资历史
![]()
数据来源:Crunchbase
Lysogene是目前世界上唯一一家致力于治疗影响中枢神经系统病变的脑内基因疗法的生物技术公司,它通过开发腺相关载体来证明向中枢神经系统安全传递遗传物质方面的有效性,针对具有中枢神经系统参与和高度未满足的医疗需求的严重遗传病理学开发突破性治疗。
公司目前的主打产品是是LYS-SAF302和携带人N-硫葡糖胺磺基水解酶(hSGSH)的rAAV-rh.10。通过直接注射到大脑中,产品能刺激分解硫酸乙酰肝素的酶的产生,目前适应症有用Ⅱ型粘多糖贮积症(MPS ⅢA)或Sanfilippo综合征A型,目前正准备采用其下一代基因治疗配方启动Ⅱ/Ⅲ期关键临床试验;基于AAV的GM1神经节苷脂病基因疗法处于临床前开发阶段
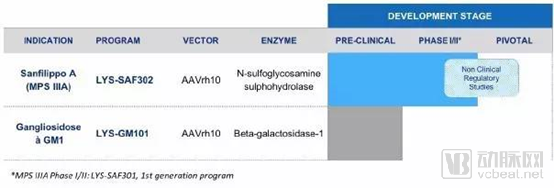
Lysogene公司研发管线(来源:公司官网)
2018年,Lysogene与Sarepta Therapeutics达成合作协议,前者拥有在美国和欧洲以外市场商业化LYS-SAF302的独家权利,后者拥有在欧洲商业化LYS-SAF302的独家权利。
信念医药创立于2018年,创始人肖啸长期从事基因治疗药物及其载体的研发及应用,特别是AAV基因载体的改进及高滴度高纯度生产工艺、简易安全高效的基因载体及直接注射技术的研发,在基因治疗领域具有15年以上的研究和产业化开发经验。公司将专注于基因治疗药物及其载体的研发和产业化,A轮融资情况如下:贝瑞基因出资2,000万元、夏尔巴一期出资4,000万元、极创金源出资1,000万元。
基因编辑公司
Sangamo公司成立于1995年,原名Sangamo Biosciences。总部位于美国加州Richmond,于2000年公司上市。公司的核心技术是锌指核酸酶(ZFN)基因编辑技术和ZFP-TF基因调控技术,专注于遗传性代谢疾病、血液学疾病、中枢神经系统疾病药物的研究。其产品SB-913是首个ZFN在体基因编辑候选产品,目前正在Ⅰ/Ⅱ期临床试验中被评估用于治疗粘多糖贮积症Ⅱ型(MPS Ⅱ,亨特综合征)。
Sangamo Therapeutics融资历史
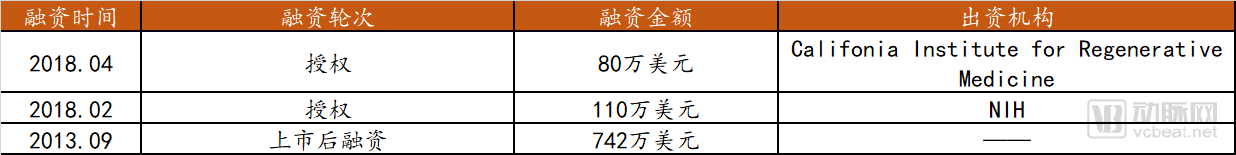
数据来源:Crunchbase
公司凭借基因编辑领域相对而言发展最为成熟的技术及其专利,与多家药企都开展了合作。
除了上文提到与辉瑞的两次合作之外, 2018年2月,Gilead旗下公司Kite与Sangamo Therapeutics宣布,两家公司已经达成全球合作,使用Sangamo的锌指核酸酶(ZFN)技术平台开发下一代肿瘤离体细胞治疗。Sangamo将获得1.5亿美元的预付款。基于使用Sangamo技术的10多个产品的研发、监管和推广里程碑的实现,Sangamo有望获得高达30.1亿美元的潜在付款。
2018年5月,Sangamo和赛诺菲子公司Bioverativ合作开发治疗镰状细胞病的候选体外基因疗法BIVV003。同时Sangamo正与英国制药巨头Shire合作开发针对亨廷顿蛋白HTT的基因疗法,目前该疗法正在进行临床前研究,Shire将负责包括IND申请在内的临床开发活动。
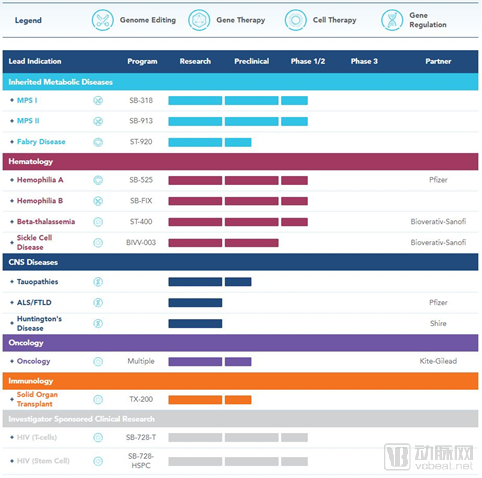
Sangamo产品研发管线(来源:公司官网)
Editas Medicine成立于2013年,总部位于美国马萨诸塞州,创始人包括CRISPR技术开发的领军人物、华人科学家张锋。Editas Medicine于2016年在NASDAQ上市,据招股书披露,公司拥有相关领域内的21项专利,同时还有200项专利正在申请中,其中核心专利由张锋授权至Editas。基于CRISPR/Cas9基因编辑技术平台,公司致力于通过改变患者的致病基因以实现相关疾病的治疗。目前其管线包括眼睛、肌肉、血液疾病以及肝病、肺病和癌症多个领域。
Editas Medicine融资历史
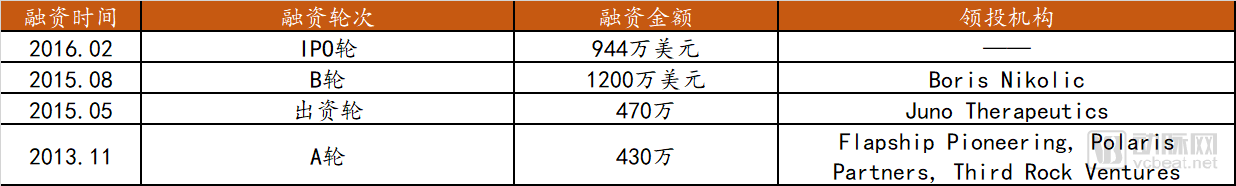
数据来源:Crunchbase
2019年7月,Editas Medicine和Allergan联合宣布正式启动CRISPR疗法AGN-151587的Ⅰ/Ⅱ期临床试验。试验计划招募18名Laber先天黑朦10(LCA10)患者以验证CRISPR疗法的安全性、耐受性和疗效。该试验为全球首个在人体内进行的CRISPR基因编辑试验。
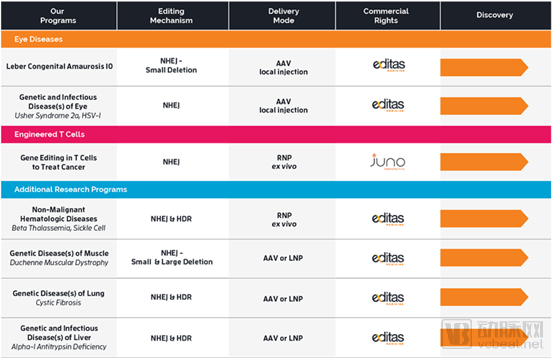
Editas Medicine产品管线(来源:公司官网)
CRISPR Therapeutics成立于2013年,由CRISPR技术先驱Emanuelle Charpentier创办,总部位于瑞士,研发中心在美国马萨诸塞州,公司于2016年上市。CRISPR Therapeutics的产品管线使用CRISPR/Cas9基因编辑技术治疗血液、肌肉以及肿瘤等多种疾病。
CRISPR Therapeutics融资历史
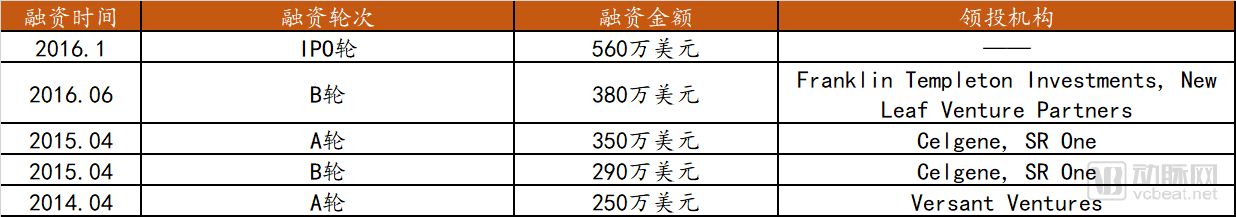
数据来源:Crunchbase

CRISPR Therapeutics研发管线(来源:公司官网)
CRISPR Therapeutics与Vertex于2015年签署协议,Vertex最多可获得6个CRISPR疗法,CTX-001是第一个。双方将对这一疗法共同开发和商业化,并且平分全球的研发成本和利润。
CTX-001在体外通过电穿孔的方式将CRISPR系统引入患者CD34+ HSC并回输,从而治疗β-地中海贫血(TDT)和镰状细胞病(SCD)。2018年8月,该疗法在欧洲的Ⅰ/Ⅱ期临床试验正式启动,该临床试验为欧盟批准的首个由制药公司发起的临床试验。同年10月,FDA批准了CTX-001用于治疗SCD的IND;2019年1月和4月,FDA分别授予CTX-001快速通道指定,用于治疗SCD和TDT。
CRISPR Therapeutics还和拜尔成立的一家对半持股的合资企业Casebia Therapeutics,目前该公司已经启动A型血友病和SCID的临床前研究。
除了上述产品研发管线,CRISPR Therapeutics于2018年9月宣布与致力于糖尿病再生医学的ViaCyte公司达成协议,结合各自的技术开发能够有效治愈I型糖尿病的干细胞衍生胰岛替代疗法,扩展了基因编辑技术在其他自身免疫疾病上应用的可能性。
Intellia Therapeutics于2014年创办,总部同样位于美国马萨诸塞州。创始人包括CRISPR先驱Jennifer Doudna,公司于2016年上市。
Intellia Therapeutics融资历史
数据来源:Crunchbase
2015年1月,Intellia Therapeutics与诺华展开了一项长达五年的研发合作计划,共同利用CRISPR研究造血干细胞相关的疾病治疗研究及CAR-T细胞治疗产品,适应症包括TDT以及SCD等。2018年12月,Intellia扩大了与诺华的细胞疗法合作,包括眼部干细胞产品。
与诺华的合作使得Intellia拥有了独特的脂质体纳米颗粒(LNP),将其作为体内基因编辑的递送载体。LNP递送及CRISPR/Cas9编辑的效率已有部分临床前数据证明,双方合作的SCD项目处于后期临床前阶段。
2016年4月,Intellia与Regeneron(再生元)公司达成了6年的合作协议,Regeneron向Intellia支付7500万美元预付款,并同意在Intellia下一轮股权融资时投资5000万美元。目前双方合作的针对转甲状腺素蛋白淀粉样变性(ATTR)研究产品处于临床前研发阶段。
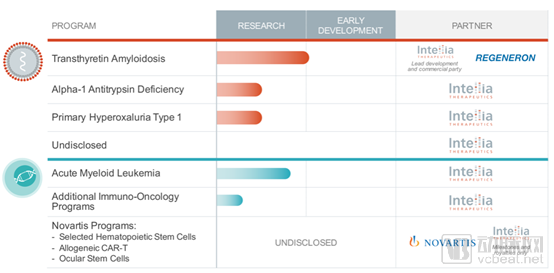
Intellia Therapeutics研发管线(来源:公司官网)
博雅辑因成立于2015年,创始人为北京大学研究员魏文胜。基于体外及体内基因编辑技术相关自有专利,EdiGene拥有多条产品研发管线,包括β地中海贫血等多种遗传性疾病及针对恶性肿瘤的通用型CAR-T疗法等。并且,EdiGene已建立起数千平米GMP级别基因编辑治疗产品开发及实验基地。
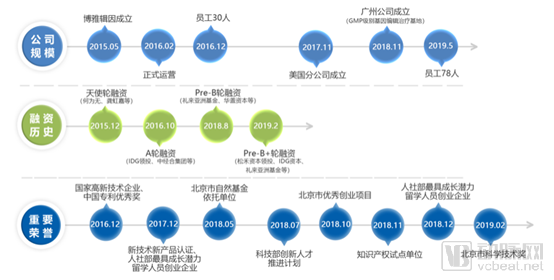
EdiGene公司简介(来源:公司官网)
随着研发管线的不断成熟,EdiGene与多家医院及临床医生团队建立了稳定的研发合作关系。药物开发方面,EdiGene拥有融合AI技术的高通量基因组筛选平台及大量基因编辑相关自主知识产权。筛选平台产生的生物大数据可高效准确地为药物及疗法搜索疾病靶点,同时精准划分用药人群,在药物早期开发及后期临床研究过程中,为创新药企提高效率、节约时间及人力成本。目前公司已进行到Pre-B轮融资。
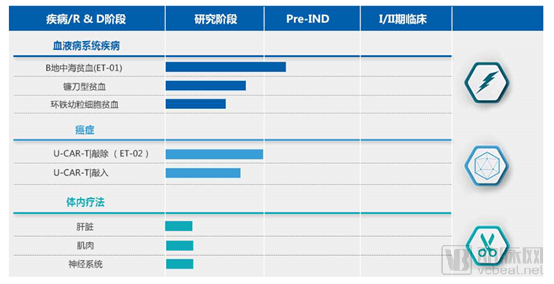
博雅辑因研发管线(来源:公司官网)
主要参考文献
1. Wang D, Tai PWL, Gao G. Nat Rev Drug Discov. 2019 May;18(5):358-378.
2. Anguela XM, High KA. Annu Rev Med. 2019 Jan 27;70:273-288.
3. High KA, Roncarolo MG. N Engl J Med. 2019 Aug 1;381(5):455-464.
4. Gaj T, Gersbach CA, Barbas CF 3rd. Trends Biotechnol. 2013 Jul;31(7):397-405.
5.Dunbar CE, High KA, Joung JK, Kohn DB, Ozawa K, Sadelain M. Science. 2018 Jan 12;359(6372).
6. Miller JC, Patil DP, Xia DF, Paine CB, Fauser F, Richards HW, Shivak DA, Bendaña YR, Hinkley SJ, Scarlott NA, Lam SC, Reik A, Zhou Y, Paschon DE, Li P, Wangzor T, Lee G, Zhang L, Rebar EJ. Nat Biotechnol. 2019 Aug;37(8):945-952.
7. Paschon DE, Lussier S, Wangzor T, Xia DF, Li PW, Hinkley SJ, Scarlott NA, Lam SC, Waite AJ, Truong LN, Gandhi N, Kadam BN, Patil DP, Shivak DA, Lee GK, Holmes MC, Zhang L, Miller JC, Rebar EJ. Nat Commun. 2019 Mar 8;10(1):1133
8. Miller JC, Tan S, Qiao G, Barlow KA, Wang J, Xia DF, Meng X, Paschon DE, Leung E, Hinkley SJ, Dulay GP, Hua KL, Ankoudinova I, Cost GJ, Urnov FD, Zhang HS, Holmes MC, Zhang L, Gregory PD, Rebar EJ. Nat Biotechnol. 2011 Feb;29(2):143-8
9. Wang H, La Russa M, Qi LS. Annu Rev Biochem. 2016 Jun 2;85:227-64.
10. Fellmann C, Gowen BG, Lin PC, Doudna JA, Corn JE. Nat Rev Drug Discov. 2017 Feb;16(2):89-100
11. Gammage PA, Viscomi C, Simard ML, Costa ASH, Gaude E, Powell CA, Van Haute L, McCann BJ, Rebelo-Guiomar P, Cerutti R, Zhang L, Rebar EJ, Zeviani M, Frezza C, Stewart JB, Minczuk M. Nat Med. 2018 Nov;24(11):1691-1695
12. Bacman SR, Kauppila JHK, Pereira CV, Nissanka N, Miranda M, Pinto M, Williams SL, Larsson NG, Stewart JB, Moraes CT. Nat Med. 2018 Nov;24(11):1696-1700
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。