
# 热门搜索 #
Florence :增长最快的临床试验工具,进一步探索区块链应用于临床试验
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持根据Grand View Research的研究报告称,到2025年,整个EDC的市场将达到11.6亿美元。比起成本的节省,由于新药研发平均周期超10年。药企和CRO企业更看好的是EDC系统可以缩短决策时间,从而加速药物研发。
此外,随着精准医疗时代的到来,药物针对一种非常特殊的疾病或者某种基因识别的疾病,临床试验的复杂度增加了3倍,如果不采用自动化软件,临床试验根本难以进行。到目前为止,EDC系统在北美发展得最好,国外临床研究机构EDC采用率高达90%。这主要因为在美国对EDC系统有着更高的认知水平和严格的临床信息处理监管规范。
在整个市场中,已经有了巨头的身影,例如和 Medidata Solutions竞争激烈的甲骨文公司,精鼎医药的BioClinica。蛋糕虽大,但是不亚于虎口夺食。
Florence作为一家初创企业能够在EDC市场中抓人眼球的原因,首先是因为它搭上了大热的区块链列车,其次是它现在已有2000家临床试验站点。Florence在2016年完成首轮融资,融资170万美元。
Florence成立于2014年,它与创新的临床试验机构合作,通过易于使用和适应性强的软件消除基于站点的临床试验操作延迟。电子化数据采集的需求是巨大的,当其他医疗部门朝着整合数字流程的方向发展时,临床试验却继续停滞不前,还得依赖于文件夹和分散的电子系统。
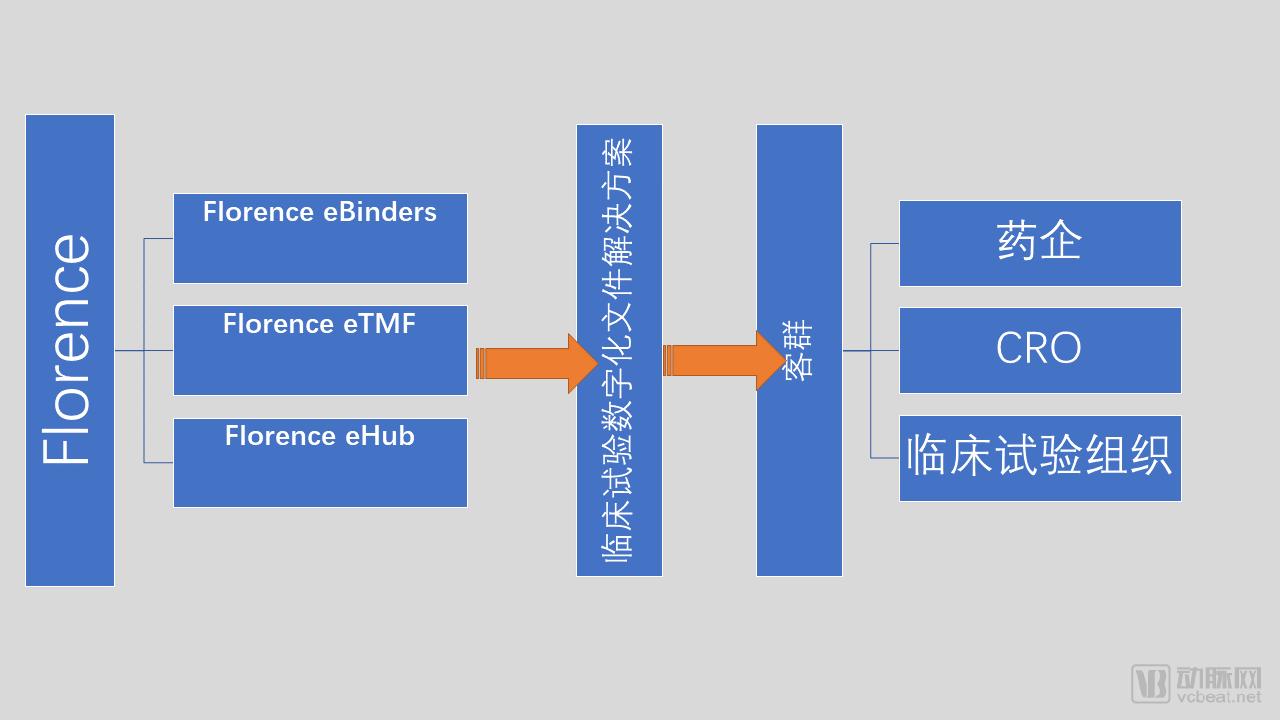
该公司旗下的产品主要包括Florence eBinders、Florence Etmf、Florence eHub。Florence eBinders可以通过领先的数字管理方案、数字资源管理方案和合同管理解决方案加速临床试验工作流程。消除向研究临床试验站点发送邮件、电子邮件和创建临床试验文档和协议的需要。
eRegulatory和eSource解决方案的采用在2015年和2016年进展缓慢,各大临床试验机构都在等着看该技术是否具有已证明的投资回报。随着早期的临床试验机构采用EDC系统的积极影响越来越明显,整个行业开始行动起来。2017年,使用Florence的临床试验机构增长了近300%。
完全使用了Florence的eBinders的临床研究机构发现,它们的研究启动时间平均快了20%,文档周期时间减少了40%——使得临床试验站点能够在不增加运营人员的情况下扩大研究容量。这些数据来自Florence官网,目前使用Florence系统的临床试验涵盖了600多个主要疾病领域。
使用Florence eHub的制药公司和临床试验机构,Florence的解决方案为临床研究机构和药企之间搭建起了桥梁,可以节省多达25天的研究启动时间——可能会节省数百万美元,使新药或设备更早上市,从而挽救生命。
在新药研发这个平均耗时10年以上,花费过10亿的领域,EDC能提供的最大价值就在于减少研发周期。此外,赞助商可以通过与他们的跟踪站点建立永久的数字连接,立即度量和应对合规问题,从而将合规风险降到最低。
2018年4月,Florence宣布超过2000个临床试验机构正在使用Florence旗下的eBinders来加速临床试验研究,同时配套使用eRegulatory和eSource。
Florence在去年与区块链资产担保公司Verady宣布建立了合作关系,开发用于推进医疗和临床研究的医疗区块链应用。Verady的应用程序编程接口(API)将提供一个易于使用、标准化的Representational State Transfer, (ReST)接口,以便为Florence的客户抽象出区块链的复杂性。该合作伙伴将与几家制药公司共同开发开放源码区块链应用程序,用于管理病人和临床试验数据。
Florence是临床研究中增长最快的工作流程工具,为数千名临床研究人员和临床试验发起者管理病人和试验数据。Verady开发的技术使得通过区块链进行资产担保更加容易和安全。
Florence CTO Andre garcia在一份声明中说:“Florence-verady合作项目允许研究临床研究机构和制药公司通过区块链对患者数据进行更多的控制。通过Verady API管理的患者和临床试验数据允许研究团队在尊重患者权利的同时,利用海量的患者数据。”
在不牺牲隐私、安全或透明度的前提下,将大量信息保持在一起的能力将是一项飞跃,它将有助于简化临床数据的收集、存储和提交过程。可以极大地减少管理临床试验所需的资源。想象一下,在一项临床试验中,研究人员可以获得与他们试验相关的特定健康数据,而另一组研究人员可以获得一组与单独试验相关的特定数据。临床试验机构可以看到数据来自他们的注册者,受试者(和他们的医生)可以看到他们所有的医疗记录数据来自办公室访问、可穿戴设备和病人报告的结果。所有这些都可以在不牺牲病人隐私的情况下实现。
IBM做了一项调查,预计到2020年,大多数医疗保健管理人员将对区块链技术进行重大投资。根据今年3月,动脉网蛋壳研究院发布的报告《医疗区块链产业报告》中总结的8大区块链加医疗的应用场景中,其中一项就是临床试验。
2016 年卫生经济学杂志的一篇文章报道说,制药公司花了 10 多年和 26 亿美元才让一款药物上 市。可见,药物研发所需的成本、精力和时间很难估量。这些成本中的大部分是由于过度复杂的 多机构行政和临床试验管理问题所造成的。利用区块链可以管理来源于多个试验场所、多个试验 患者的实验结果数据进行评审及管理,降低多中心试验时的试验成本。

Florence创始人Ryan Jones
Florence的CEO兼创始人Ryan Jones毕业于达特茅斯学院,拥有加州伯克利分校的MBA学位。在加入Florence之前,Ryan是Pubget的总裁,该公司被美国版权结算中心(CopyrightClearance Center)收购,这是一个为全世界600多家医院和研究机构的临床医生服务的研究平台。
Ryan从微软的企业搜索组加入了Pubget,在微软他的主要成就是帮助网站用搜索技术让信息变得可以理解和访问。在微软之前,Ryan在风险投资机构Commonwealth Capital Ventures分析了企业软件投资,并在扬基集团(Yankee Group)建立了技术市场策略。《纽约时报》(New York Times)、《华尔街日报》(Wall Street Journal)和哈佛商学院出版社(Harvard Business School Press)都引用了他的演讲。
联合创始人Andres Garcia曾在VMware AirWatch做产品经理。VMware AirWatch致力于提供企业移动化管理的解决方案。最早毕业于桑坦德工业大学大学的Andres Garcia曾在爱科集团(AGCO Corporation)任职10年。Andres Garcia热衷于用技术解决日常问题。
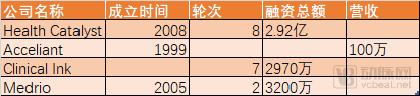
数据来自crunchbase 单位:美元
Health Catalyst
Health Catalyst公司正在解决美国一些顶级医疗系统的医疗数据仓库问题。经过8轮融资,共融资2.92亿美元。
随着纸质记录向电子记录的转变,组织健康数据、理解它、并迅速完成它已经成为一个挑战。Catalyst帮助组织、规范化和链接来自所有不同系统的数据。通过使用丰富的元数据功能,用户甚至非技术用户都可以搜索到它。
这使您能够将您的数据用于复杂的操作、财务、临床和研究报告需求——快速地为每个人提供他们想要的答案的能力。
Acceliant
Acceliant公司为全球CRO企业、制药和医疗器械企业提供eClinical trial解决方案。
Acceliant公司为生命科学、CROs和pharma提供实时、综合的临床试验解决方案,提供工具和专业知识,帮助它们做出明智的决策。它的eClinical套件允许用户构建研究、设计电子病例报告表单eCRFs、通过多个来源(EDC)获取数据、直接从患者ePRO获取数据,以及管理其他临床数据管理功能。目前营收在1000万美元左右。
在今年2月,Acceliant宣布和临床研究机构clinnex partner合作,加速临床试验研究。通过该合作,Clinnex将利用Acceliant的增强功能,如多试验管理,随机化,RBAC,药物供应管理,SDTM,医疗编码,文档管理系统和eCRF开发,同时优化其临床数据管理产品。
Clinical Ink
开发电子文档记录软件,用于在临床试验期间在移动设备上记录源数据。Clinical Ink集团为临床试验行业提供eSource解决方案。它提供了一个电子源解决方案SureSource,它允许用户在协议特定的eSource文档上记录注释、解释和验证源数据,并捕获协议所需的数据。该公司还提供了一个电子源记录(ESR)用于提供更清洁的数据的临床试验。此外,它还提供托管服务。Clinical Ink公司成立于2006年,总部位于北卡罗来纳州的温斯顿-塞勒姆。
经过7轮融资,Clinical Ink共融资2970万美元。
Clinical Ink 可以实时获取完整的高质量数据。SureSource捕获了源数据和eCRF研究数据,大大减少了与传统的EDC和纸质源过程相关的错误和时间延迟。在患者访问期间使用SureSource,防止数据错误,并确保站点始终使用最新的协议——提供高质量的研究数据的实时访问。
SureSource使临床医生能够在病人来访期间轻松有效地捕获研究数据。为了模拟纸张的简洁性,SureSource采用了电子平板电脑,消除了后来将纸张源文件誊写到EDC的时间和成本负担。独立调查数据始终显示,超过90%的站点更喜欢SureSource而不是纸质文档,因为它提高了站点效率——有助于改进协议执行和减少错误。
BioClinica, Inc.
BioClinica,是全球领先的集成、技术强化临床试验管理服务提供商。BioClinica支持制药和医疗设备创新与成像核心实验室,互联网图像传输,电子数据捕获,交互式语音和网络响应,临床试验管理和临床供应链设计和优化解决方案。生物临床服务在整个临床试验过程的各个阶段都能最大限度地提高效率和可管理性。经过20多年的经验和2000多项成功的试验,BioClinica公司通过最终的批准,支持了许多新药的临床开发。BioClinica公司在两大洲运营着最先进的、符合规范的成像核心实验室,并支持来自美国、欧洲和亚洲的世界各地的eClinical和数据管理服务。营收约2.018亿美元。
Medrio
Medrio提供先进的电子数据采集EDC和电子临床工具,适用于复杂的临床试验。Medrio建立在一个平台上,以此来比竞争对手更快、更低成本、更精简。自2005年以来,Medrio一直在为临床试验中的数据管理构建一个真正的SaaS解决方案。总部位于加州旧金山的Medrio公司通过智能、前瞻性、生态化的产品将控制权交到用户手中。
对于整个EDC市场的发展,未来还大有可为。由于eClinical解决方案的技术进步,市场正在快速增长,预计这将为这个行业带来未来的增长机会。此外,预计有关EDC解决方案的认识将在不久的将来促进需求。此外,卫生保健研究和质量机构和国家卫生信息技术协调员办事处等政府组织正在促进采用电子系统进行数据管理。这些因素都可以推动EDC系统在药企中的应用。
Grand View Research的研究报告中认为,未来EDC市场发展有几大趋势:
1、由于大型制药公司越来越多地采用该软件,预计该软件部分将见证利润丰厚的增长。
2、基于云计算的部分预计将实现最快的增长,因为它允许远程访问数据,并提供更大的存储空间。
3、由于制药公司在开发新药方面的研发支出不断增加,预计一期临床试验阶段的年复合增长率在预测期内将达到最快水平。
4、由于医疗设备行业主要参与者的需求不断上升,CROs在EDC系统中占据了最大的收入份额。
5、亚太地区的EDC系统市场预计将出现最高的增长率,因为该地区有大量外包公司提供成本效益高的eClinical解决方案
6、市场正面临激烈的竞争,因为有许多组织为临床数据管理提供技术高效的解决方案。公司采用并购、新产品开发、分销渠道拓展等策略,以获得竞争优势。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。