利拉鲁肽获批扩展适应症治疗儿科患者
FDA宣布扩展利拉鲁肽的适应症扩张批准,治疗10岁以上的2型糖尿病患者。
拉鲁肽是一款GLP-1类似物。
该批准主要基于利拉鲁肽在成人患者中的临床试验结果,及在10岁以上儿科患者的安慰剂对照组临床试验结果。
试验数据显示,利拉鲁肽治疗组糖化血红蛋白水平降低超过7%的比例较安慰剂组更高(64% VS 37%)。
君联医疗全球新药资讯速递 · 第10期
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持
2019.6.17-2019.6.23,本周新药数据共14个,其中肿瘤6个,代谢疾病及罕见病各2个,肝病、关节炎、精神病和抗生素各1个。
利拉鲁肽获批扩展适应症治疗儿科患者
FDA宣布扩展利拉鲁肽的适应症扩张批准,治疗10岁以上的2型糖尿病患者。
拉鲁肽是一款GLP-1类似物。
该批准主要基于利拉鲁肽在成人患者中的临床试验结果,及在10岁以上儿科患者的安慰剂对照组临床试验结果。
试验数据显示,利拉鲁肽治疗组糖化血红蛋白水平降低超过7%的比例较安慰剂组更高(64% VS 37%)。
创新GLP-1抑制剂治疗减肥手术后低血糖
获突破性疗法认定
Eiger Biopharmaceuticals宣布FDA授予其在研药物Avexitide突破性疗法认定,该药物用于治疗减肥手术后的低血糖。
Avexitide是一款创新GLP-1受体拮抗剂。
54名患者接受了治疗。
与安慰剂给药对照组相比,治疗组的餐后血糖水平得到了显著提高,急性治疗需求降低。
第一三共口服白血病药物日本获批上市
第一三共宣布该公司开发的口服FLT3抑制剂Vanflyta(quizartinib)在日本获批上市,用于治疗携带FLT3-ITD编译的复发难治性急性骨髓性白血病患者。
Vanflyta是一款口服FLT3抑制剂。
获批基于名为QuANTUM-R的关键性全球3期临床和一项在日本患者中开展的2期临床试验结果。
与挽救化疗相比,Vanflyta显著改善了患者的总生存期(6.2个月 VS 4.7个月)。
罗氏不限癌种的个体化疗法日本获批上市
罗氏不限癌种的个体治疗药物Rozlytrek(entrectinib),在日本获批治疗携带NTRK基因融合的晚期复发实体瘤患者。
Rozlytrek是一款针对NTRK和ROS1基因融合设计的特异性酪氨酸激酶抑制剂。
批准基于包括STARTRK-2关键性2期临床试验、STARTRK-1和ALKA-372-001的1期临床试验的多项临床试验结果。
试验数据显示,ORR达57.4%,DOR为10.4个月。
Amgen双抗药物Blincyto显著延长白血病患者OS
Amgen公布了双抗Blincyto(blinatumomab)治疗急性淋巴性白血病患者的5年积极长期疗效数据。
Blincyto是一款利用Amgen双特异性T细胞接合器平台开发的靶向CD19和CD3的双抗分子。
在名为BLAST的2期临床试验中,入组患者已接受过3轮以上化疗,但仍有癌细胞残留。
中位随访期59.8个月时,中位OS为36.5个月,其中76%的患者接受治疗后转为最小残留疾病MRD指标转为阴性。
图:Blincyto作用图示
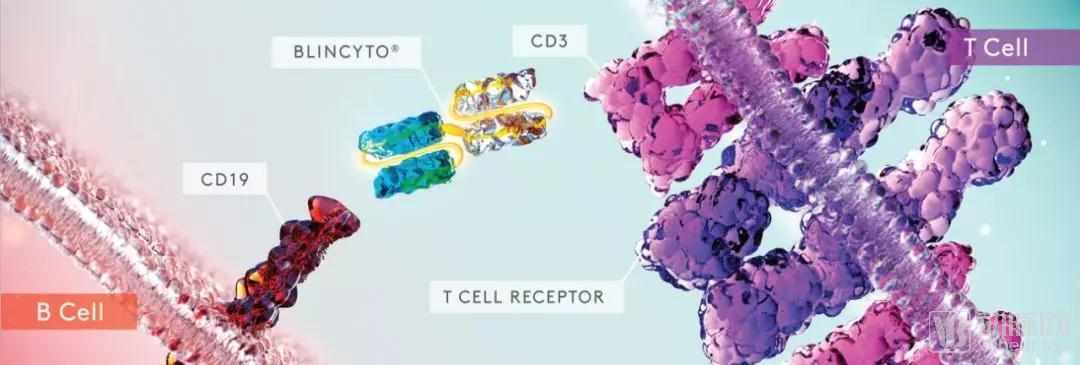
来源:Amgen
可逆性BTK抑制剂治疗淋巴癌效果初显
ArQule公司宣布其在研产品BTK抑制剂ARQ531在复发难治性B细胞淋巴瘤患者的早期临床实验中结果积极。该药物有望解决第一代BTK抑制剂的耐药性问题。
APQ 531是一款可逆的第二代BTK口服抑制剂。
开放标签、单臂、剂量递增的临床1期试验正在进行中。
APQ 531在安全性、药代动力学、抗肿瘤活性方面表现良好。
阿斯利康PARP抑制剂奥拉帕利
获欧盟批准一线治疗BRCA突变卵巢癌
阿斯利康宣布旗下PARP抑制剂Lynparza(奥拉帕利)在欧盟获批一线治疗BRCA突变的晚期卵巢癌患者。
奥拉帕利是一款PARP抑制剂。
此次批准基于随机、双盲、安慰剂对照的多中心3期临床试验SOLO-1。
截至随访41个月的时间点,奥拉帕利治疗组中位PFS尚未达到,安慰剂组这一指标为13.8个月。同时奥拉帕利治疗组有60%的患者在治疗36个月内病情没有进展,安慰剂组的这一比例为27%。
科济生物宣布其BCMA CAR-T疗法IND获批
科济生物自研BCMA CAR-T疗法 CT053近日获得FDA的IND批准,成为国内原研CAR-T项目首个独立在美国获得IND的项目。
该疗法是科济生物自主研发的,采用全人抗体靶向BCMA的CAR-T疗法。
临床试验尚未开展。
临床试验尚未开展。
阿斯利康COPD三联疗法全球首获日本批准上市
阿斯利康宣布其慢性阻塞性肺病的三联疗法Breztri Aerosphere 日本获批上市,这也是这款三联疗法的全球首次获批。
Breztri Aerosphere是布地奈德、格隆溴铵、富马酸福莫特罗三种活性成分组成的三联疗法。
批准基于1900名中重度阻塞性肺病患者参与的、名为KRONOS的随机双盲3期临床试验。
试验数据显示,该三联疗法相比对照组能够显著改善患者肺功能。
Melinda广谱抗生素Baxdela提交sNDA
Melinta Therapeutics公司宣布,公司向FDA递交了广谱抗生素药物Baxdela(delafloxacin)sNDA,并获得了优先审评资格。该sNDA希望申请扩展适应症至治疗社区获得性细菌性肺炎(CABP)
Baxdela是一款创新广谱抗生素,对革兰氏阴性和阳性菌都具有效力,并可治疗耐甲氧西林金黄色葡萄球菌。
该申请基于随机双盲3期临床试验的结果。
试验结果表明,Baxcela相比莫西沙星在疗效上达到非劣效性标准。
抗衰老新药治疗骨性关节炎结果积极
UNITY Biotechnology在研抗凋亡蛋白抑制剂UBX0101,在治疗中重度膝关节骨性关节炎的1期试验中取得积极结果。
UNITY是一款抗凋亡蛋白,能够选择性的去除产生衰老细胞。
临床1期试验的主要终点是安全耐受性。
试验结果显示,生物标志物的改变与衰老细胞的消除和组织环境的潜在改善一致。
诺和诺德Esperoct欧盟
获批治疗青少年和成人A型血友病
诺和诺德长效化凝血因子VIII Esperoct在欧盟获得上市许可,用于治疗12岁以上青少年和成人的A型血友病。
Esperoct是一种凝血因子FVIII的浓缩物重组形式。
Esperoct进行了A型血友病中最大的预登记临床试验,270名已接受过治疗的严重A型血友病患者参与了临床试验。
试验结果显示,Esperoct可以减少出血发作频率、预付和控制出血事件。
Alnylam全球首个RNAi药物日本获批上市
Alnylam宣布旗下RNAi药物Onpattro在日本获批上市,用于治疗遗传性转甲状腺素(hATTR)淀粉样变性伴多发性神经病。Onpattro18年8月获FDA批准上市,这也是全球首个获批的RNAi药物。
Onpattro是一种RNAi药物,能够阻断甲状腺素运载蛋白的生成。
批准基于随机、双盲、安慰剂对照的全球临床3期试验APOLLO。
试验结果表明,Onpattro改善了患者的神经功能、生活质量、日常生活活动能力、步行能力、营养状况、自主神经症状,达到了主要终点及所有次要终点。
图:Onpattro结构
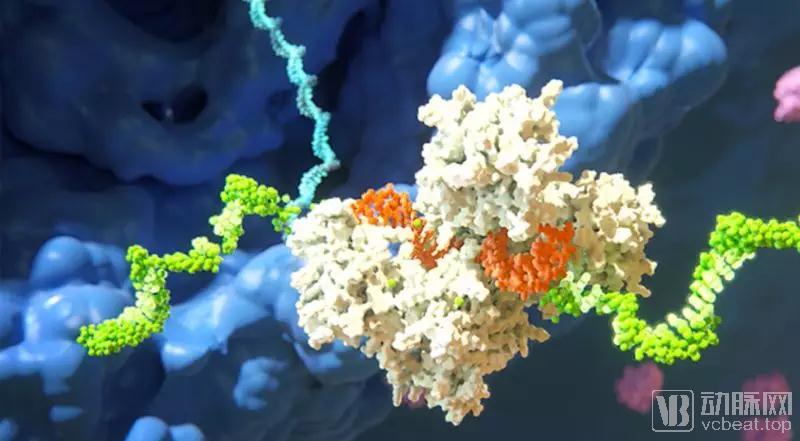
来源:Alnylam
住友制药Lonasen Tape
成全球首个获批抗精神病药物透皮贴片
住友制药宣布旗下Lonasen Tape(blonanserin,布南色林)透皮贴片在日本获批上市,这将是全球首个透皮贴片剂抗精神病药物。
Lonasen片剂和粉剂2008年即在日本上市,本次上市的贴片技术来自于日本电工株式会社。
本次透皮贴剂的获批基于一项多国多中心、随机、安慰剂对照、双盲3期研究和一项长期单臂、开放标签、持续治疗研究。
试验数据显示,Lonasen Tape能够显著降低主要终点PANSS评分,能够达到与片剂类似的给药效果。
❖默沙东在近日的投资者大会上表示Keytruda还处于研发早期阶段,目前K药有超过1000项临床试验在开展中,下一个研发目标是作为辅助疗法治疗早期癌症。
❖Bluebird bio公布了其最近获得欧盟批准的输血依赖性β-地中海贫血基因疗法Zynteglo(LentiGlobin)的价格为177万美元,成为目前全球第二昂贵的药物,仅次于诺华脊髓性肌萎缩症基因疗法Zolgensma的210万美元。但由于生产商的问题,该药物的上市继续推迟。
❖吉利德科学宣布与Nurix公司签署战略合作协议,双方将利用Nurix专有的泛素/E3泛素连接酶平台,开发创新蛋白降解药物,治疗癌症及其它具有挑战性的疾病。
❖辉瑞公司近日宣布以114亿美金价格收购Array公司,Array公司以激酶抑制剂为核心平台,主要资产是治疗黑色素瘤的BRAF/MEK抑制剂组合Braftovi/Mektovi。
❖据路透社报道,GSK计划出售部分非核心的产品以支付和辉瑞的消费健康领域整合成本,这些计划被出售的产品包括部分拉丁美洲、欧洲药物授权及Physiogel护肤品牌。
❖赛诺菲宣布将在法国、德国裁剪466个岗位,以重组研发团队,将研发重心聚焦癌症、免疫学、罕见病和疫苗领域。赛诺菲还表示将停止心脏病学适应症的新研究,并将糖尿病研究的重点缩小至解决疾病根源的药物。
❖赛诺菲旗下公司Genzyme宣布停止与基因治疗公司Voyager的合作项目,这两项研发项目是针对亨廷顿舞蹈病的基因疗法VY-HTT01以及针对遗传性共济失调的基因疗法VY-FXN01。17年赛诺菲已经放弃了与Voyager合作帕金森基因治疗VY-AADC的计划。
❖百济神州宣布与SpringWorks Therapeutics共同成立MapKure公司,合作开发百济自研临床前药物BGB-3245,这是一款针对特定单聚体和二聚体B-RAF激活突变型的口服高选择性小分子抑制剂,具有治疗多种实体瘤的潜力。
❖索元生物宣布获得芬兰奥利安集团阿尔茨海默病新药ORM-12741开发、制造、商业化的全球权利。这是一款靶向α-2C肾上腺素受体创新选择性拮抗剂,迄今已开展了11项临床研究。
❖恒瑞宣布以750万美金预付款+900万美金研发里程碑付款+不超过9200万美金的销售里程碑付款的价格获得Mycovia专利先导化合物VT-1161在中国的开发、注册、生产、销售独家授权。VT-1161是由Mycovia研发的新型口服小分子选择性真菌CYP51抑制剂,用于治疗复发性外阴阴道念珠菌病。
❖康方药业宣布与正大天晴共同成立合营公司,共同开发康方生物自研PD-1抗体AK105。正大天晴出资3.45亿元人民币,康方生物以知识产权和技术权益作为无形资产出资,双方各占50%股份,正大天晴将获得AK105的独家销售权。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。