
# 热门搜索 #
未来细胞疗法揭秘,NK细胞可能成为T细胞的抗癌协同者,已有公司涉足
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持2019年3月19日至3月21日,在圣地亚哥举行的Innate Killer峰会上,工业和学术领域的科学家们展现了他们的细胞疗法最新研究成果。其中,一些科学家正在研究如何通过基因修饰,让自然杀伤细胞(NK细胞)表达嵌合抗原受体(CARs),形成类似于CAR-T细胞的CAR-NK细胞,从而实现靶向治疗。动脉新医药整理、编译了Innate Killer峰会中肿瘤领域的前沿疗法——NK细胞免疫疗法。
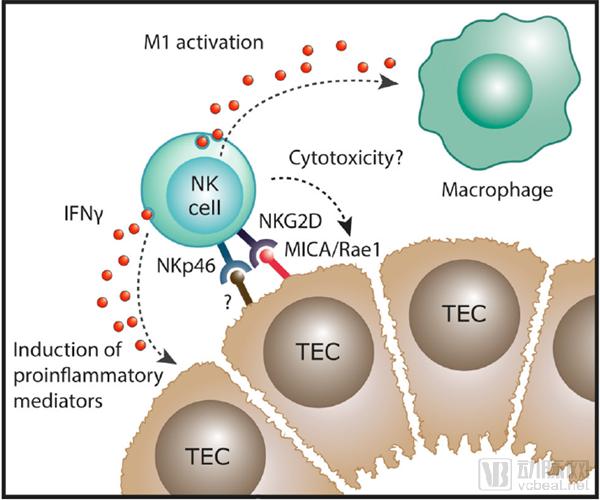
美国基因和细胞治疗协会把细胞疗法定义为“用活细胞治疗患者疾病的疗法”。在肿瘤领域,细胞疗法主要是指用基因工程修饰或无修饰的T细胞的特异性免疫治疗。随着人们对先天免疫系统有了更深层次的理解,细胞疗法的主体也从T细胞扩展到了NK细胞。NK细胞将成为T细胞的协同或替代品,靶向并消除肿瘤细胞。
贝勒医学院儿科血液肿瘤学助理教授、医学博士Robin Parihar指出:“CAR-T细胞之所以在血癌治疗领域有显著疗效,是因为肿瘤细胞及其抗原存在与血液之中。而在实体瘤中,抗原通常隐藏在体内难以发现。因此,所有细胞疗法对实体瘤疗效甚微。”
另一方面,实体肿瘤的肿瘤微环境中存在内源性免疫抑制细胞,包括髓样抑制细胞、抑制性巨噬细胞和调节性T细胞(Tregs)等,这些细胞共同抑制了包括CAR-T细胞在内的所有T细胞的活性。
最开始的时候,Parihar实验室试图改变肿瘤微环境,即减轻内源性免疫抑制,从而让CAR-T细胞疗法生效。但在研究中,Parihar实验室找到了一种制备CAR-NK细胞的新方法。这种CAR-NK细胞可以表达一种融合蛋白,融合蛋白由NKG2D(NK细胞表面的一种跨膜受体蛋白,活化型受体)和具有细胞毒性的T细胞受体ζ链两部分组成。在同种异体的肿瘤微环境——人神经母细胞瘤细胞的组织培养中,这些NKG2D.ζ细胞可以靶向并杀死骨髓免疫抑制性细胞。
与先前改变肿瘤微环境的方法不同的是,这些NKG2D.ζ细胞没有脱靶毒性,并且在首次使用后可以持续两周缓解免疫抑制。因此,NKG2D.ζ细胞将有助于CAR-T细胞在肿瘤组织募集,从而发挥抗肿瘤活性。
西奈山伊坎医学院肿瘤科学助理教授Amir Horowitz博士通过人类白细胞抗原(HLA)分子晶体来研究NK细胞。HLA基因是基因组中形态最为多样化的基因,人们对它的认知是可以刺激CD8 + T细胞。但鲜为人知的是,HLA基因可以调节NK细胞功能。Horowitz表示,这可能是因为NK细胞是先天免疫的一部分,而不是适应性免疫。它们没有先天特异性,但在骨髓中,NK细胞会受到HLA1的基因表达调控。
Horowitz使用质谱流式细胞术重新分类HLA等位基因,定义了癌症的新类别。HLA-E(人类白细胞抗原)是NKG2A形成的受体复合体的主要配体,NKG2A不同于活化型受体NKG2D,是NK细胞表达的抑制性受体。受到HLA-E刺激的NK细胞功能会被抑制,因此肿瘤微环境中具有较低HLA-E的患者的NK细胞功能不会受到抑制,这类“热”肿瘤适合使用PD-1和其他免疫疗法治疗。相反,具有较高HLA-E的肿瘤微环境呈免疫抑制性,NK细胞受到抑制,细胞浸润低。这可以解释为什么只有约10-20%的患者对PD-1疗法有初始疗效。以HLA分子作为生物标记物,重新分类患者,以“将人们划分为最有可能从现有疗法中获益的人。”Horowitz表示,“这是一种个性化的治疗方案,但不像CAR-T细胞那样具有特异性,制备耗时长。”
哥伦比亚大学儿科助理教授Emily M. Mace博士也展现了她的研究内容:研究细胞之间作用的本质以及细胞迁移在塑造功能成熟的NK细胞中的作用。
Emily M. Mac指出,由于NK细胞的产生很少受到免疫组织的限制,因此,推动NK细胞发展的动力不足。理想情况下,研究促进NK细胞发育的接触依赖因子,就可以更好地设计出基于NK细胞的免疫疗法。研究表明,随着NK细胞在在体内发育越来越成熟,NK细胞也变得越来越活跃,其发育程度取决于NK细胞和支持性基质细胞之间“突触发育”的形成。然而,她也强调,小鼠和人类的先天免疫力存在差异,因此两者对比十分困难。因为先天免疫系统是由其环境塑造的,与其环境中的微生物组、病毒组情况息息相关。在无菌小鼠中的研究结果可能不适用于人类。
CytoSen Therapeutics的联合创始人兼CSO Robert Igarashi博士则认为,将NK细胞转化可行性的细胞疗法,最重要的是生产和维持相当高的剂量。Robert Igarashi 表示:“正常成年人有十亿至二十亿个循环NK细胞,我们的剂量是10倍。”CytoSen通过IL-21刺激NK细胞扩增,与之前的方法相比,IL-21刺激的方法可以更快地产生免疫活性更强的NK细胞。
CytoSen通过将特异性的纳米粒子与IL-21连接,并与细胞外蛋白质一起嵌入预制的干净生物膜中,刺激而不是培养NK细胞。因为培养细胞通常来源于肿瘤部位的活体组织,因此可能承担伦理责任,造成污染。
“这是一种激活NK细胞的新方法。”Igarashi表示,“这种方法看起来像NK细胞的细胞膜,但避免了培养细胞的风险,且更加安全,符合欧洲的法规。这种方法也不需要数加仑的细胞培养基,因此更具成本效益和后期处理优势。纳米粒子也很容易地储存。”
在九十年代早期,Lawrence Lamb在从事博士后研究期间发现,大约四分之一的白血病患者在接受无αβT细胞的骨髓移植后,γδT细胞水平升高。而且这些患者在骨髓移植后存活率不同。
Lamb 是Incysus Therapeutics公司的CSO,在他的职业生涯的早期,他发现了这一现象,并跟进研究,进而证实γδT细胞可以杀死实验室中的血癌细胞系。但γδT细胞十分少见,且难以直接作用于血癌细胞。Lamb花了大约10年时间才研究出如何在体外扩增γδT细胞,从而大规模生产并用于临床。
“γδT细胞和NK细胞很相似。”Lamb表示,“γδT细胞的优越之处是它们没有主要组织相容性复合物,因此可以识别许多NK细胞不能识别的东西。γδT细胞还具有不同的激活和抑制受体库,因此它们可能比NK细胞更具在不同的环境的适应性。”Incysus已经制备了γδT细胞,并与化疗药物替莫唑胺(Temodar)联合使用。化学疗法使肿瘤微环境对γδT细胞更敏感,γδT细胞进而募集其他先天免疫细胞进一步攻击肿瘤。Incysus将在今年晚些时候研究这种疗法对胶质母细胞瘤的疗效。Lamb预测,γδ T疗法离肿瘤治疗越来越近,这种疗法并不是取代CAR-T疗法,而是在其他肿瘤疗法之后,无法检测到肿瘤细胞时,通过“免疫系统增强”,彻底根除疾病。
麻省理工学院生物学教授、红细胞生成领域先驱Harvey Lodish博士也带来了研究突破:在实验室中用造血干细胞生产成熟的红细胞(RBC)。Lodish将其RBC技术带到Flagship Pioneering,Flagship Pioneering发现了一种表达治疗性蛋白质的有核前体细胞的生产方法。这种方法为细胞疗法提供了新思路,这也是Rubius Therapeutics的起源。
成立五年后,Rubius Therapeutics已经开发出成熟的红细胞疗法Red Cell Therapeutics™(RCTs)。Rubius从非O型血中提取CD34 +祖细胞,提取成功率高达95%。然后通过慢病毒载体将遗传物质递送至前体细胞,接着在生物反应器中培养和扩增。细胞成熟后,细胞核就会消失,这就是RCTs疗法。RCTs疗法有几种潜在应用:治疗罕见的酶缺乏症、治疗肿瘤以及自身免疫疾病。
Rubius总裁Torben Straight Nissen博士坚信一个观点:“未来的细胞疗法是同种异体的。”Rubius的红细胞都来自通用供体的前体细胞,因此公司的产品都具有同种异体的特性。此外,Rubius的红细胞可以储存并随取随用,且可以低频、低剂量给药。红细胞循环周期长达120天。
Rubius的第一个目标是罕见疾病苯丙酮尿症(PKU)的治疗。Rubius近期设计了一项试验, PKU患者将接受Rubius的RTX-134的治疗,RTX-134将在RCT平台表达苯丙氨酸解氨酶(PAL),从而分解苯丙氨酸。
此外,Rubius正在研究RCTs在高胱氨酸尿症和难治性痛风等其他酶缺乏疾病,以及癌症和自身免疫性疾病的应用。
总的来看,细胞疗法早已不再局限于基于T细胞的修饰或改造的疗法,而是拓展到NK细胞、γδT细胞、红细胞等疗法领域。在NK细胞疗法领域,美国的NantKwest已然成为行业巨头。
NantKwest成立于2002年,总部位于美国加州。2015年7月,当时只有11名员工和3个尚未盈利的技术平台的NantKwest在纳斯达克上市,IPO募集2.07亿美元,并在上市首日涨幅40%,市值达27亿美元。NantKwest致力于使用NK细胞治疗癌症、传染性疾病和炎症性疾病,拥有haNK、taNK和t-haNK三个技术平台。目前,NantKwest的癌症管线已经在美国、加拿大和欧洲开展了临床I期试验。
反观国内,NK细胞治疗领域较少有企业涉足,其中,诺康得生物专注于NK细胞、巨噬细胞新型免疫检查点抑制剂新药研究,并以NK细胞为载体,开创了基于非病毒的糖化学细胞治疗平台(sugar cell),其CECT-NK疗法通过对NK细胞进行神经氨酸修饰,从而靶向癌细胞诱导凋亡。
图片来源:Jan-Eric Turner,Constantin Rickassel,et al.Natural Killer Cells in Kidney Health and Disease.Frontiers in Immunology.10,587(2019).
参考链接:https://www.genengnews.com/insights/natural-killer-cells-emerge-as-an-anticancer-alternative-to-t-cells/
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。