
# 热门搜索 #
惠大生物永生化DC-CTL技术弥补CAR-T多重技术短板,有望解决实体肿瘤治疗难题
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持永生化DC-CTL技术是一项细胞免疫治疗领域的创新技术,目前正在中国人民解放军总医院开展临床研究。这是该技术全球首次进行临床研究,截至目前已完成了第一阶段安全性试验,部分患者生存质量QOL评分有所提高。有效性研究还在进展之中。
动脉网(微信号:vcbeat)记者采访了在纽约州立大学Albany分校获得分子生物学博士的邵永平教授,并获悉了新技术永生化DC-CTL技术的最新进展。
邵教授目前是北京惠大生物科技有限公司(简称:惠大生物)首席科学家,曾参与十余项国内外的重大课题研究,在Cancer Ressearch、Immunity等核心期刊发表论文近四十篇,并参与了普通高等教育“十三五”规划教材《分子细胞生物学》的编写。
据了解,永生化DC-CTL技术突破了多年来困扰免疫学发展和免疫细胞抗癌技术的瓶颈,有望彻底攻克癌症。该技术在应对乙肝、艾滋病、禽流感以及中东呼吸综合征等疾病方面也有广阔应用前景。
永生化DC-CTL技术原理
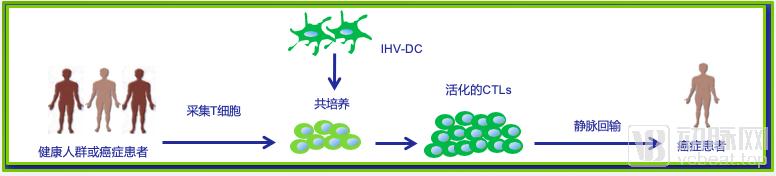
永生化DC-CTL技术原理示意图
通过使用与患者HLA相符、表达实体瘤特异性抗原或新抗原的永生化DC细胞株体外激活患者T细胞,使其进行大量扩增并激活成为以特异性CD8+T细胞为主的细胞毒性淋巴细胞(CTLs),针对肿瘤进行特异性杀伤。
永生化DC-CTL技术相对CAR-T技术的差异
首先,永生化DC技术的靶点不会受限,无论胞内还是胞外的靶点,都可以被DC细胞识别。其原因在于DC细胞的作用机制,DC细胞遇到抗原时,会直接将其捕获,再消化成一段段的肽段呈递到细胞表面,再与表面的MHC结合激活T细胞进行免疫反应。
惠大生物目进行的肺癌临床试验,靶点正是胞内蛋白(MAGEA3蛋白),它在肺癌病人组织中特异表。这时 CAR-T技术对于这种靶点的疾病束手无策,而永生化DC-CTL技术没有对胞内外靶点的限制,对于此类疾病同样可以进行永生化DC技术的细胞治疗。
其二,永生化DC-CTL技术不需要筛选‘子弹头’。邵教授解释道:“永生化DC-CTL技术不再需要去筛选抗体库,我们直接去克隆肿瘤特异性表达的蛋白对应的基因,再将其插到DC细胞中即可。”永生化DC-CTL技术只需从病人身上获取肿瘤细胞特异性表达的蛋白,让DC细胞也表达这种蛋白,随后便能“教会”T细胞识别该肿瘤,并攻击这类肿瘤细胞。
其三,与CAR-T技术相比,永生化DC-CTL技术最明显的一点优势在于它属于DC细胞天然刺激T细胞,而非人为刺激T细胞产生免疫反应,这样模拟了细胞内刺激T细胞扩增的环境,效率自然也会更高。邵教授告诉记者:“在较短的时间内,我们就可以刺激T细胞扩增十倍甚至百倍,大大缩短临床前的准备工作。”
不再直接对CAR-T进行“操刀改造”,而去改造T细胞的上游DC细胞,将未经任何人为改造的T细胞回输到人体体内,这也是更安全和有效的。
永生化DC技术蓝海广阔
目前,在国内外做DC细胞免疫治疗的很多,但做永生化DC免疫治疗的却屈指可数。邵教授说道:“在国内,只有一家科研机构在做永生化DC学术层面的研究,和惠大生物一样将技术落实到临床研发的,我们还没找到第二家。”
在国外,有一家法国和比利时的合资公司,也正在做永生化DC技术的临床落地。不过该公司的永生化DC细胞并非自己制备的,而是从一个罕见病人的体内提取的“天然永生化DC细胞”。
该公司后续操作也和惠大生物相同,导入抗原基因,激活T细胞,然后再回输到患者体内。不过因为这是唯一的一株天然永生化细胞,让这家公司的所有研发都是围绕这一株细胞展开,只有单一的配型治疗,对于与该DC细胞不配型的肿瘤则无法进行治疗。而惠大生物的永生化DC细胞是通过人为改造而来,目前已有十余种DC细胞的配型。
曾在2016年,美国Back Bay公司就曾言,永生化DC技术是一个估值过亿的新技术。在这片蓝海,惠大生物最先走了进来。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。