
2019.6.10-2019.6.16,本周新药数据共15个,其中肿瘤8个,糖尿病及皮肤病各2个,肝炎、关节炎和罕见病各1个。
❖K药进一步扩大适应症范围,获批一线治疗晚期头颈癌,可单药一线治疗表达PD-L1的患者,或与化疗联用一线治疗全部晚期头颈癌患者群体。2016年FDA基于ORR数据批准K药用于铂基化疗后复发的头颈癌患者后仍要求K药提供更多临床获益数据,而此次获批主要基于试验中OS的获益。
❖基因泰克的抗体偶联药物Polivy加速获批上市,成为全球第6个获批ADC。较标准疗法,该药物能够将复发难治性DLBCL患者的CR提升一倍至40%。此前ADC一直被诟病治疗剂量窗口短和容易脱靶,进展不多,但近2年ADC领域不断有新的进展出现,从2017年开始有4个ADC药物上市,而且都是在液体瘤领域,该赛道是否已经出现系统性的投资机会值得思考。
❖再生元披露双特异性抗体REGN1979的1期结果,针对FL和DLBCL的ORR分别为93%和57%,而且有2例DLBCL患者在 CART疗法失败后获得了CR。CD3/CD20双抗与CART都是通过调动T细胞杀伤癌变的B细胞,但是CD19和CD20这2个靶点显示出了不同的作用效果。未来若CD3/CD20双抗针对液体瘤的数据持续不错,考虑到其成本相对较低,很有可能会对CART疗法形成较大压力。
❖受关注的CymaBay公司的PPAR激动剂Seladelpar临床2b期失败,当天CymaBay公司股价暴跌50%。Seladelpar未能实现主要临床终点MRI-PDFF优于安慰剂组的改善,虽然在肝损伤生化指标上有较好表现,仍被认为难以说服FDA,基本可以判断出局。另一款PPAR激动剂,Genfit的在研NASH药物Elafibranor受此影响前景亦不乐观。
百济神州更新替雷丽珠单抗
治疗复发或难治性经典型NHL中国患者
的关键性2期临床研究结果
百济神州在EHA年会上更新了抗PD-1抗体替雷利珠单抗用于治疗复发/难治性经典型霍奇金淋巴瘤中国患者的关键性2期临床研究结果。
替雷利珠单抗是百济神州一款在研抗PD-1人源化单克隆抗体。
单臂、多中心的替雷利珠单抗单药治疗复发/难治性经典型霍奇金淋巴瘤中国患者的关键性2期临床研究入组了70位先前接受过自体造血干细胞移植治疗失败、或者接受了至少两项经典型霍奇金淋巴瘤系统治疗的患者。
截至数据节点,ORR为87.1%,CR为62.9%,中位PFS未达到。
基因泰克抗体偶联药物Polivy
获FDA加速批准上市
基因泰克的抗体偶联药物Polivy(polatuzumab vedotin-piiq)获FDA批准上市,与苯达莫司汀与rituximab联合使用治疗难治性弥漫性大B细胞淋巴瘤成人患者。这也是首款针对DLBCL的化疗免疫药物。
在1b/2期实验中,80名患有复发或难治性DLBCL的患者入组接受治疗。
试验结果表明,该款创新组合疗法的CR达到40%,传统疗法的CR为18%。
和黄中国索凡替尼治疗
晚期非胰腺神经内分泌瘤
达到3期临床主要终点
和黄中国开发的多机制创新抗癌药索凡替尼(surufatinib,HMPL-012),在治疗晚期非胰腺神经内分泌瘤的关键性3期临床试验提前达到预先设定的主要终点。
索凡替尼是具备多种作用机制的抗癌新药,可以通过抑制血管内皮生长因子受体(VEGFR)和成纤维细胞生长因子受体(FGFR)来抑制血管生成,还可以抑制集落刺激因子-1受体调节肿瘤相关巨噬细胞,促进免疫反应。
名为SANET-p的中国3期临床试验。
索凡替尼已经成功达到PFS的预设主要疗效终点,具体结果将于近期学术会议上公布。
Blueprint Medicines
四线胃肠道间质瘤疗法提交NDA
Blueprint Medicines公司宣布为Avapritinib向FDA递交了NDA,用于治疗携带PDGFRA外显子18突变的胃肠道间质瘤成人患者,或作为四线疗法。
Avapritinib是具有高选择性的口服KIT/PDGFRA抑制剂
截至 2018年11月16日,共纳入 237 例患者,包括 111 例四线及以上的胃肠道间质瘤患者和 43 例 PDGFRA外显子18突变患者。
试验结果显示,PDGFRA外显子18突变患者群体ORR达86%,四线治疗胃肠道间质瘤患者的ORR为22%。
再生元双特异性抗体REGN1979
早期临床试验结果积极
再生元在EHA大会上宣布,其在研双特异性抗体REGN1979,在治疗复发/难治性B细胞非霍奇金淋巴瘤患者的早期临床试验中取得积极结果。
REGN1979是靶向CD20和CD3的双特异性抗体。
截至2019年3月,81名患者纳入评估。
ORR达93%,CR达71%,CAR-T疗法失败的患者也能达到完全缓解。
图:REGN1979结构
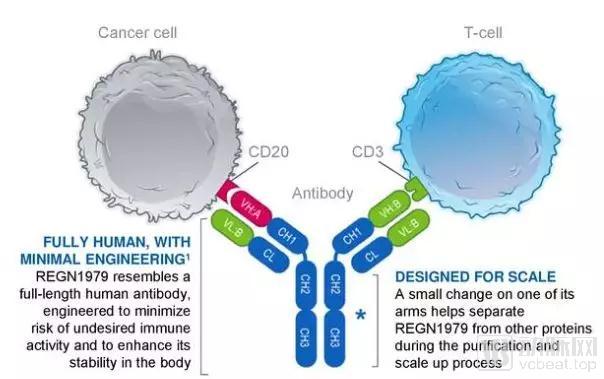
来源:再生元公司展示材料
Keytruda获批一线治疗晚期头颈癌
Keytruda近日获FDA批准,作为单药一线治疗表达PD-L1的晚期头颈癌患者。此外,K药也可联合常用化疗方案,对晚期头颈癌患者进行一线治疗。
K药是一款PD-1抑制剂。
批准基于名为KEYNOTE-048的关键3期临床试验。
试验数据显示,Keytruda单药在表达PD-L1的患者中显示出了OS获益;不考虑PD-L1表达情况下,Keytruda与化疗组合也能起效。
新基CD19 CAR-T细胞疗法Liso-sel
治疗淋巴瘤数据积极
新基公布了其抗CD19 CAR-T细胞疗法lisocabtagene maraleucel (liso-cel,JCAR017)治疗复发难治性非霍奇金淋巴瘤患者的最新分析数据。
Liso-cel是对一款靶向CD19抗原、以4-1BB为共刺激区的CAR-T细胞疗法。
该研究是一项开放标签、多中心I期研究。
试验数据显示,全部剂量水平的ORR为71%,CR为53%。
新基JAK2抑制剂Fedratinib
治疗原发性或继发性骨髓纤维化效果强劲
新基近日公布了旗下在研JAK2抑制剂Fedratinib治疗原发性或继发性骨髓纤维化的2期临床数据。
Fedratinib是一款JAK2抑制剂。
一项单臂、开放标签、在原发性或继发性骨髓纤维化患者中开展的2期临床试验。
经过6个治疗周期,有31%的病人脾脏体积缩小≥35%,症状缓解率≥50%的患者比例为27%。
艾伯维类风湿性关节炎新药
Upadacitinib3期结果积极
艾伯维在研JAK1抑制剂Upadacitinib,在治疗中重度类风湿性关节炎的3期试验中取得积极结果。
Upadacitinib是一款具有高度选择性的第二代JAK抑制剂。
SELECT-EARLY试验和SELECT-COMPARE试验。
临床试验数据显示,经过48周治疗,Upadacitinib患者组中达到临床缓解标准的比例显著高于活性对照组。
诺华苏金单抗治疗银屑病
2年疗效数据积极
诺华宣布,旗下苏金单抗在治疗银屑病关节炎的追踪试验中,展现出长期持续抑制患者的疾病进展的效果。
苏金单抗是全球首个获批的全人源抗IL-17A单抗。
996名银屑病关节炎患者参与了该3期FUTURE 5追踪试验
300 mg组和150 mg组分别有89.5% 和82.3%的患者实现了2年以上无放射影像学进展的关键临床终点。
罗氏利妥昔单抗治疗寻常型天疱疮
第2项3期研究取得积极顶线数据
罗氏宣布,利妥昔单抗治疗寻常型天疱疮在第2项3期研究PEMPHIX中取得了积极顶线数据。
利妥昔单抗是一种人鼠嵌合单抗,能与异常B淋巴细胞上的CD20抗原结合并引发B细胞溶解的免疫反应。
PEMPHIX是一项随机、双盲、双模拟、阳性对照、平行臂、多中心3期研究。
与标准治疗组相比,利妥昔单抗组更高比例患者病情获得持续完全缓解。
礼来糖尿病新药Tirzepatide 临床结果积极
将启动NASH 2b临床
礼来宣布治疗2型糖尿病的在研药物Tirzepatide临床实验结果积极。同时试验结果显示Tirzepatide可以改善NASH相关的标志物,治疗NASH的2b期研究将于今年开展。
Tirzepatide是一种具有胃抑制多肽受体和胰高血糖素样肽-1双重受体激动剂功效的生物大分子。
一项26周临床2b试验及一项12周临床2期试验。
试验数据显示,Tirzepatide显示出胰岛素敏感性标志物改善,显著降低血糖的同时能够降低体重。
诺和诺德公布两项口服索马鲁肽
3a临床试验结果
诺和诺德近日公布了口服索马鲁肽的2项3a临床试验数据。
索马鲁肽是一种天然人胰高血糖素样肽-1类似物。
名为PIONEER 2和PIONEER 4的两项临床试验。
与对照药物恩格列净相比,口服索马鲁肽治疗后糖化血红蛋白水平的降低幅度更大(0.9% VS 1.3%)。与利拉鲁肽相比,口服索马鲁肽的降低糖化血红蛋白水平也更好。
PTC治疗DMD药物Emflaza
获批扩展适应症
PTC Therapeutics治疗杜氏肌营养不良(DMD)的药物Emflaza(deflazacort)获FDA批准扩大适用范围,用于治疗2-5岁的杜氏肌营养不良患者。
Emflaza是一种糖皮质激素前体。
批准基于196名男性儿童参与的临床试验。
试验结果表明,使用0.9 mg/kg剂量Emflaza的儿童,其肌肉力量较安慰剂对照组有显著提高。但高剂量组却没有观察到获益。
治疗NASH的PPAR激动剂Seladelpar
遭遇2b临床失败
CymaBay治疗非酒精性脂肪性肝炎(NASH)的药物Seladelpar在2b期临床中未能达到主要终点,其临床收益劣于安慰剂。
Seladelpar是一款PPAR激动剂。
NCT03551522是一项双盲、安慰剂对照的2b期临床试验,以磁共振成像-质子密度脂肪分数(MRI-PDFF)作为主要终点。
Seladelpar的临床收益差于安慰剂,未能达到主要终点。
图:Seladelpar NASH 2b临床试验方案

来源:CymaBay投资者演示材料

❖苏桥生物与浙江新码生物医药就一种新一代单克隆抗体偶联药物ARX788的单克隆抗体部分的后期临床产品开发与商业化生产达成了全面战略合作协议。
❖Tessa宣布将与中新广州知识城建立合资企业,共同投资1.2亿美金,该合资企业在将成为Tessa的细胞疗法在中国研究、临床开发和商业化的唯一授权商。中新广州知识产权将以4000万美金价格获得该合资企业的13%股权。
❖药明康德新药研发和生产基地项目签约落户常熟苏虞生物医药产业园(BioBAY-常熟),将在常熟打造全球领先的CDMO基地。
❖GSK与CRISPR技术领先研究者Jennifer Doudna教授和Jonathan Weissman教授合作,创建基因组研究实验室,共同开发基于CRISPR的创新技术来迅速加快新药开发。GSK在未来5年内将为该实验室投资6700万美元。
❖Certara公司名为Simcyp的基于生理学的药代动力学模拟技术,首次被FDA用于在批准复杂仿制药的过程中代替体内临床研究证明生物等效性,这或许将为BE研究开辟一条更为安全、迅速和经济的方式。
❖丹麦哥本哈根的Genmab与Janssen宣布将共同开发新一代抗CD38单抗HexaBody-CD38。HexaBody-CD38使用了Genmab专有的环形六聚体抗体HexaBody技术。目前Genmab共有两款上市药物,分别是授权给杨森的多发性骨髓瘤药物Darzalex(daratumumab),和授权给GSK的慢性淋巴细胞白血病药物Arzerra (ofatumumab)。
❖默沙东宣布计划收购Tilos Therapeutics,并将获得后者调控TGFβ的在研抗体产品。该收购预付款+里程碑付款最高可达7.73亿美元。Tilos Therapeutics主要开发针对LAP相关肽的抗体治疗剂,用于治疗癌症、纤维化和自身免疫性疾病。
❖拜耳与基石药业达成以中国为重点的全球临床合作,双方将共同评估基石PD-L1单抗CS1001 联合口服多激酶抑制剂瑞戈非尼治疗含胃癌在内的多种癌症的安全性、耐受性、药代动力学和抗肿瘤疗效。基石药业将作为此研究的发起者,拜耳将提供试验所需的瑞戈非尼。

































