
# 热门搜索 #
首发!我国首个成功出海的全球抗癌新药百悦泽®在本土获批
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持今日,百济神州宣布,公司自主研发的新一代BTK抑制剂百悦泽®(泽布替尼胶囊)获得中国国家药品监督管理局(NMPA)批准,用于治疗既往接受过至少一项疗法的成人套细胞淋巴瘤(MCL)患者、既往接受过至少一项疗法的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)。
这标志着百悦泽成为在国内首个上市的国产BTK抑制剂,将为我国淋巴瘤患者带来高缓解率的全新治疗选择。同时,这也是继百悦泽在美国成功获批上市后,百济神州在本土与全球商业化进程中的又一重要里程碑。
百济神州中国区总经理兼公司总裁吴晓滨博士表示:“百悦泽在国内迎来两大适应症的首次获批,让我们倍感激动,这款我国史上首个出海发达市场的抗癌新药,终于在本土落地,能够为我国更多的淋巴瘤患者带来新的治疗选择。百悦泽相继在海内外成功上市,是近年来我国创新药产业崛起的又一力证,代表着我国的制药企业已经拥有充分实力,为本土患者研制国际一流品质的,可及性与可负担性更出色的创新好药,帮助我国癌症患者改善药物治疗难题。”
淋巴瘤是一组起源于淋巴造血系统的恶性肿瘤的统称,是我国常见的十大恶性肿瘤之一,也是我国和全球范围内发病率增速最快的恶性肿瘤之一。根据流行病学统计,在我国每年新发约88,200例淋巴瘤患者中,非霍奇金淋巴瘤(NHL)约占所有淋巴瘤的91%2,包括66%的B细胞非霍奇金淋巴瘤。其中,套细胞淋巴瘤(MCL)在所有B细胞非霍奇金淋巴瘤中约占5%2,而慢性淋巴细胞淋巴瘤(CLL)/小淋巴细胞淋巴瘤(SLL)约占所有B细胞非霍奇金淋巴瘤的6.4%2。
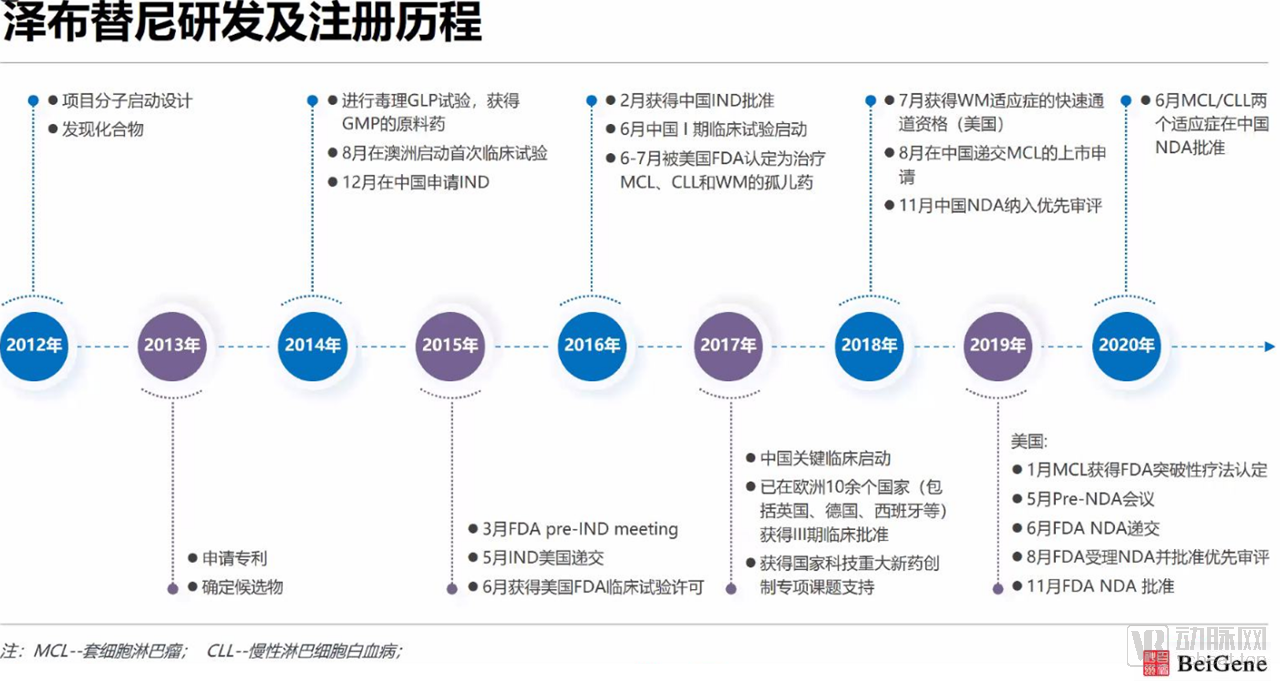
百悦泽是一款新型强效BTK抑制剂,经过分子结构的优化,能够对BTK靶点形成完全、持久的精准抑制。在一系列临床试验中,其在MCL、CLL等多种B细胞淋巴瘤中显示了良好的疗效与安全性。2019年11月,百悦泽(泽布替尼胶囊)获得FDA批准,用于治疗经治一次的套细胞淋巴瘤患者,成为我国史上首个在美获批的本土研发抗癌新药,实现了本土新药出海“零的突破“。
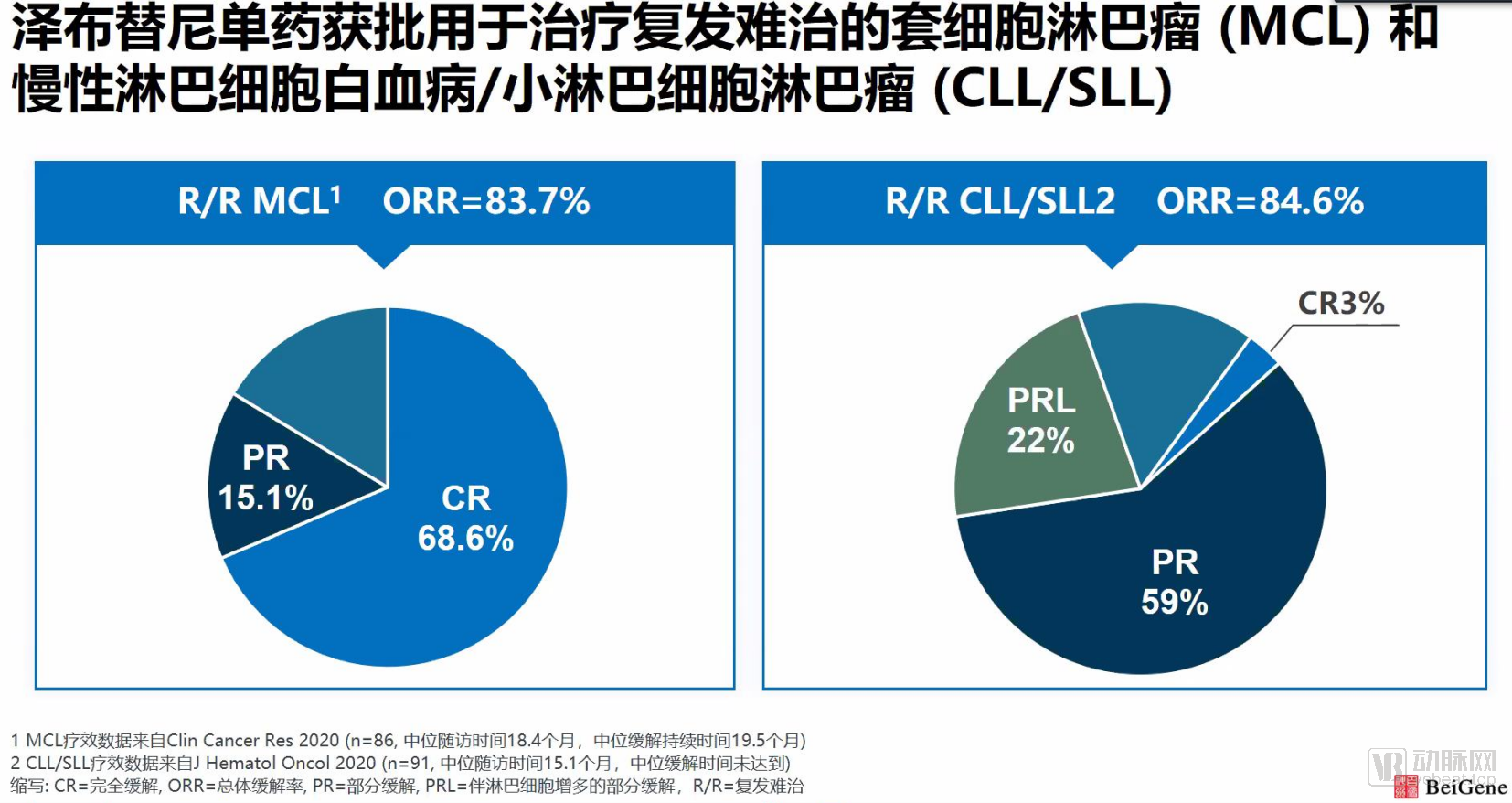
此次百悦泽在中国本土获得两项适应症的同时批准,主要是基于两项关键性临床研究的数据。一项中国的关键性2期多中心临床试验BGB-3111-206研究的数据显示,百悦泽单药治疗R/R MCL的总缓解率ORR达84%,完全缓解率达69%。而在另一项针对R/R CLL/SLL的中国关键性2期多中心临床试验BGB-3111-205研究中,百悦泽治疗的总缓解率达到62.6%,完全缓解率达3.3%,部分缓解率达59.3%,另外有另有22.0%的患者获得伴有淋巴细胞增多的部分缓解。
南京医科大学第一附属医院血液科主任、浦口慢淋中心主任李建勇教授牵头主持了百悦泽在CLL中的205临床研究,李教授介绍:“淋巴瘤是一种老年人高发的疾病,特别是慢性淋巴细胞白血病这类进展相对缓慢的亚型,不少患者的生存期可能超过十年,因此治疗方案是否安全、耐受,是我们的重要考量。我很高兴能在临床研究中,见证新一代BTK抑制剂展现的优秀疗效,并且耐受性良好,房颤、出血等发生风险非常低。相信它在国内的获批上市,能够为患者带来疗效更佳、副作用更小的治疗方案,帮助患者提高预后,进一步改善生活质量,作为临床医生,我们的治疗信心也会更足。”
北京大学肿瘤医院淋巴瘤科主任、大内科主任朱军教授介绍:“过去,由于缺少有效的治疗方案,淋巴瘤患者长期面临着用药难、用药贵的困境,治疗效果与生活质量有待提升。如今,我国在临床研究、新药研发方面不断取得突破,使我们的患者有了新的希望。作为临床医生和研究者,我很欣慰见证了我们本土研发的新一代口服靶向药百悦泽能够为患者带来更好的生存,赢得海内外专家的一致好评,相信不远的将来,会有更多来自中国生物制药公司的新药将在全球获批,我国患者的治疗选择也会越来越多。”
百悦泽诞生于百济神州位于北京昌平的研发中心。2012年6月,研究团队正式对BTK开发项目立项,经过一系列筛选与测试,最终在500多个化合物中,选定了最终候选分子,为其编号BGB-3111,意为百济神州成立后做出的第3111个化合物。
百悦泽(泽布替尼胶囊)的主要发明人之一、百济神州化学研发负责人王志伟博士介绍,“最初立项时,我们的目标很明确,要做一个选择性高、对靶点抑制非常专一的化合物。我们通过优化药物的分子结构,希望将BTK靶点的特异性结合率达到最大化,并最大程度减少脱靶现象,以降低不良反应的发生率,帮助患者在临床中得到更好的疗效和安全性。”
2013年4月,百济神州递交了专利申请。这是一项始自中国专利局的全球专利,也让百悦泽成为不折不扣的中国本土研发抗癌新药。2014年,百悦泽(泽布替尼胶囊)在澳大利亚正式进入临床阶段,同年8月,完成了全球第一例患者给药。
从实验室立项到如今成功在中美两地上市,百悦泽的研发跨越了8年历程。目前,百悦泽在全球启动的临床试验累计近25项,临床试验覆盖超过20个国家,500多位国际临床专家参与或主持了其相关的临床试验,其中,来自中国的临床专家超过70位。在全球范围内,共有超过1700位患者接受了泽布替尼胶囊的治疗。
“百悦泽从最初启动临床开始,一直践行着全球化的开发策略,在中国和海外国家同步开展临床研究,这也对我们临床试验的设计与质量提出了更高的要求。”百悦泽(泽布替尼胶囊)研发的主要领导者之一,百济神州高级副总裁,全球研究、临床运营和生物统计暨亚太临床开发负责人汪来博士介绍,“这个过程中,离不开中国与海外的众多临床医生与患者的付出,正是他们对百悦泽的信任与支持,使得它在国内外的临床研究得以顺利推进,为更多患者带来了切实的帮助。”
目前,百济神州正在全球范围对百悦泽开展16项临床研究,包括9项注册性或有望实现注册的临床试验。同时,百悦泽正在针对华氏巨球蛋白血症(WM)、CLL进行2项对比伊布替尼的全球临床3期头对头研究,是我国首个与外资药企研发产品开展直接头对头研究的本土新药。其中在WM中已经公布的头对头3期临床数据显示,泽布替尼相比伊布替尼,取得了更高的缓解率,以及更高的安全性与耐受性优势。
百悦泽自进入临床试验阶段以来,先后在国际和国内获得多项认定,先后获得中国NMPA优先审评认证,囊括了美国FDA优先审评的四项大满贯,又陆续被中美临床指南纳入淋巴瘤治疗的专家推荐之列。
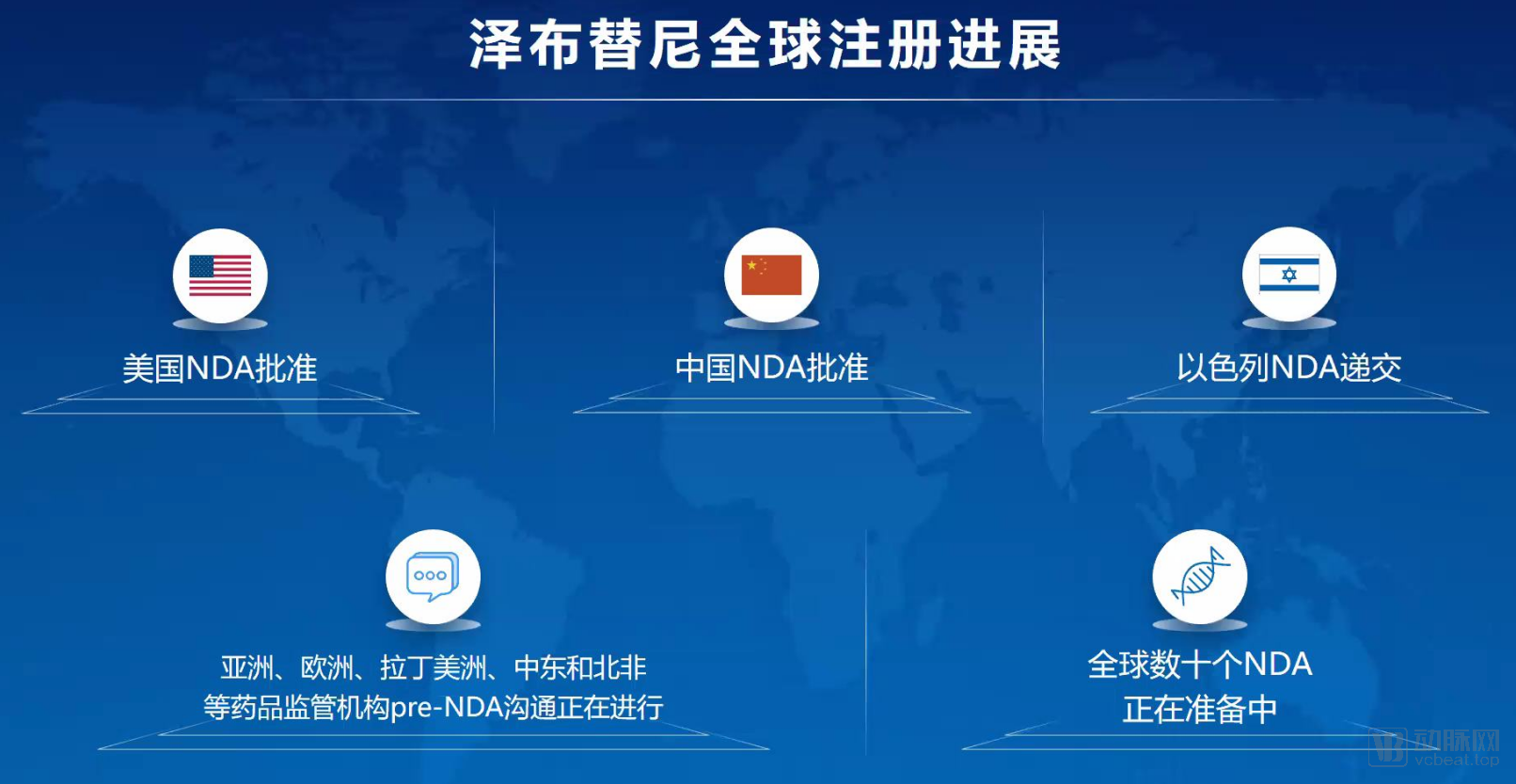
继中国和美国之后,百悦泽近期也在以色列递交了新药上市申请,并已得到受理。根据此前公布的计划,公司今年还将与欧洲药品管理局(EMA)展开沟通,加快推进百悦泽全球范围的上市进程。
百济神州高级副总裁、全球药政事务负责人闫小军女士介绍:“得益于临床试验中取得的出色数据,我们与多个国家的药监部门开展了密切的沟通,希望能将这款具备全球一流品质的新药带给更多国家的患者。在这个过程中,我们非常感谢中国与美国药监部门对百悦泽寄予的肯定,在中美两地的先后获批,为我们积累了丰富的经验与基础,将帮助我们更好地推进在其他国家地区的申报工作。”
百济神州总裁吴晓滨博士表示,“目前,百济神州已在产业链的各个环节做好充分准备,确保获批后第一时间的生产供货。作为一款本土研发、获得国际认可的高品质新药,相信它将以更高的可及性、可负担性帮助到我国的患者,同时,我们期待与国家医保部门展开沟通,推动百悦泽尽早纳入医保目录,为国内患者带来福祉,促进医保基金的良性运转。”
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。