
# 热门搜索 #
德勤报告:孤儿药、肿瘤治疗、首创新药备受关注,新资本市场下的生物医药创新未来有4个趋势
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持本文摘选自德勤报告:《资本市场回顾与展望——创新药驱动下的医药与生物科技行业》
承接上文,随着更多企业在在香港生物科技板上市 , 熟悉和偏好生物科技公司的的投资者群体确立 , 香港生物科技板将更加成熟 。香港市场有望与美股市场等量齐观。加之较为成熟的美股市场以及A股科创板确立,全球医药及生物科技的投融资活动将保持热度。
在并购方面,大型制药公司一直需要对其产品线进行更新,以应对降价压力和专利悬崖的不利影响。此外,大型制药公司普遍而言之于研发型的生物科技公司更擅长于在新药研发后期及上市后应对监管要求以及市场销售的处理,并以此去的商业上的丰厚回报。因此,以获取收到专利保护的创新药为主要动因的并购活动热度也不会有所消减。
在此过程中,我们可以观察到以下趋势:
1、首创新药持续收到资本市场关注;能够有效降低研发风险和维护市场独占性的首创新药将备受青睐;
2、新药中特殊药品、孤儿药、生物制品及肿瘤治疗将继续成为热点;
3、大型跨国生物制药公司与新兴生物制药公司开展多元化合作,将催生新的优秀企业,并在资本市场崭露头角;
4、创新药迎来全球化时代,生物科技公司倾向于去的全球开发权力后快速在全球多中心展开临床研究,以在药物获批后占领更多市场。
在创新药领域,First-in-class、Me-better以及Me-too等概念常常被提起。严格来讲,这些概念并非精确的定义,但可以生动的给创新药贴上标签,帮助人们意会一款创新药的若干特点,因此被普遍使用。
不同于Me-better和Me-too新药,首创新药在作用机理、适应症和分子实体等方面均有重大突破,可以与之进行类比的包括FDA在FDCA的505(b)(1)中描述的新药审批中新分子实体(NME)、新化学实体(NCE)等。首创新药为企业带来的潜在收入巨大,受到的竞争较少,来自政府、舆论以及供求各方面的降价压力也较小,将持续收到资本市场的关注。
首创新药往往都是全球首创,为企业带来的巨大收益也体现在全球市场的回报上,也将受到全球资本市场的关注。其主要风险主要来自漫长的研发时间、巨大的研发投入以及较高的研发风险,因此在技术或者业务模式上能够有效的缩短研发周期、节约研发投入或者降低研发风险的企业,将备受关注。
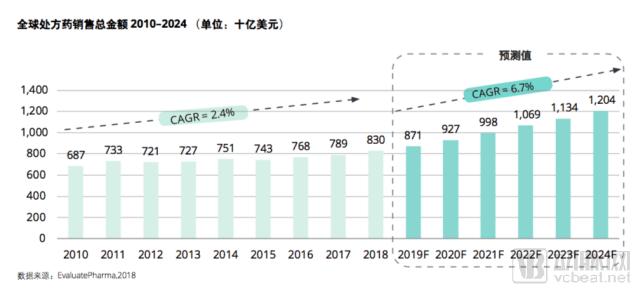
2018年全球处方药销售额已经达到8,300亿美元,预计这一数字将在2024年增至1.2万亿美元,以年复合增长率6.7%高速增长。值得注意的是,2010–2018年复合增长率仅为2.9%,增速较为平缓。2019-2024年预期复合增长率较之出现了2倍以上的大幅增长1;未来能解决当下关键需求的创新药推向市场将成为推动全球药品支出增长的关键动因。
尤其在中国,药品采购改革旨在控制中国整体药品支出:国家医保目录于2017年迎来了最近一次更新,预计目录中采用的创新药将推动创新药企业绩的显著增长。然而由于4+7带量采购的改革,仿制药(甚至Me-too新药)企业都将迎来更激烈的竞争,预计仿制药企增速较前将放缓。
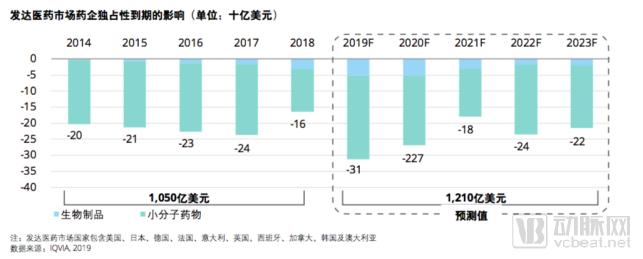
IQVIA预计2019年发达市场品牌创新药独占期到期的预期影响将达到峰值,于过去5年的1050亿美元相比显著增长,上升比率为15.2%。在未来5年总共带来1210亿美元的影响。
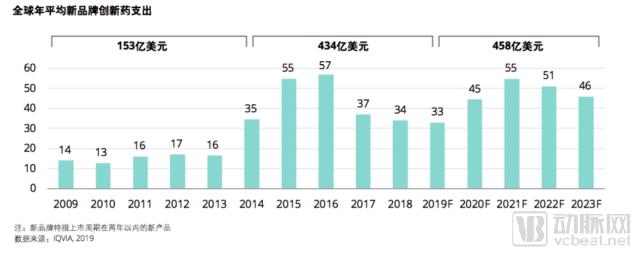
根据IQVIA 的预测,在过去五年中,创新药的数量和支出大幅增加。2014年至2018年间,新品牌创新药的平均药品支出为434亿美元 。2019年至2023年期间推出的新产品预计总支出略高,约为458亿美元 。
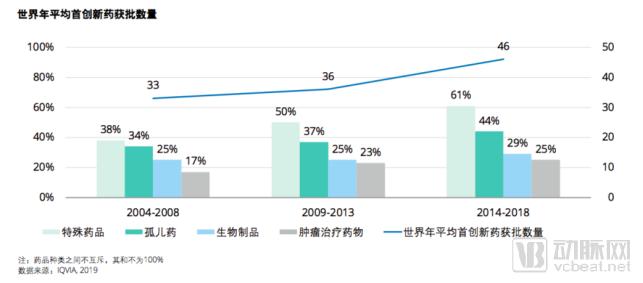
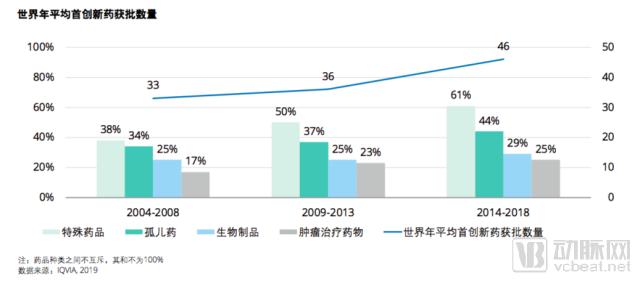
随着首创新药产品上市数量的增加,药品类型持续倾向于特殊药品 、 孤儿药、生物制品及肿瘤治疗药物。预计未来五年,特殊药品将占新推出药品的近三分之二,肿瘤治疗药物约占30%。
假设正在进行的研究和获得突破性疗法的孤儿药获批速度与历史相同 ,则未来五年孤儿药可占新发布首创新药数量的45%1。 预计未来在特殊药品、孤儿药、生物制品和及肿瘤治疗药物中,将有更多使用生物标志物( Biomarkers)来定位和治疗特定患者的医药公司。
在这一趋势下,关注于上述新药研究的公司将持续成为资本市场和并购市场的热点。
根据德勤研究 ,大型生物制药公司新药研发回报率水平已至9年新低,仅为1.9%。对于每年研发投入过百亿美元的跨国制药公司而言,高强度的研发投入未必可带来较高的回报,投资者更多关注公司当下产品以及在研管线及未来业绩的的成长性2。
研发回报率的下降,催生了大型制药企业于研发型生物科技公司之间显著的分工,越来越多的研发工作有生物技术公司完成。
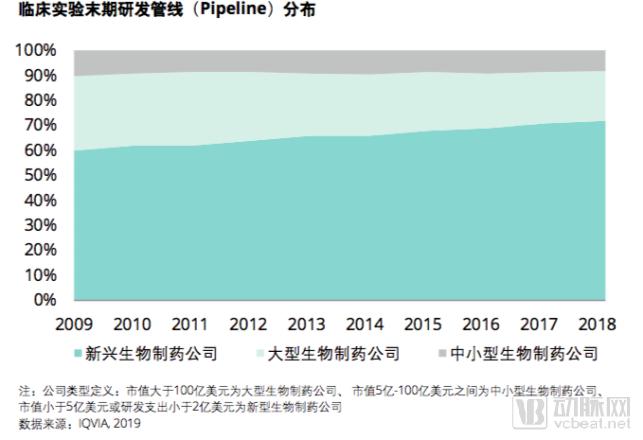
新兴生物制药公司在临床实验末期研发管线数量和首创新药获批数量持续加强。根据IQVIA 的研究 ,在过去十年中,年收入低于 5 亿美元或年研发支出不足2 亿美元的公司新兴生物制药公司临床实验末期研发管线占比已从2009年的60%增加到2018年的72% 。
在过去五年中在全球范围内成功推出了68种首创新药,较更早的一个五年( 2009-2013)的47种有大幅上升3。
在此大背景下,大型制药企业除了延续目前的兼并和收购趋势外,还将与新兴生物制药公司达成形式多样的合作关系。
模式一:与大型制药公司合作开发,可以拿到首付款和里程碑式付款。这些现金流在研发产品没有上市之前,对于人才、研发及公司运营来说至关重要。
信达生物
根据公开信息,信达生物两次与美国礼来制药达成产品开发战略合作,获得首付及潜在里程碑款等33亿美元。双方就三个肿瘤免疫治疗双特异性抗体药物等全球开发签署合作协议,里程碑付款总金额超过10亿美元,成为中国迄今为止金额做大的生物医药国际合作项目其中包括肿瘤免疫治疗的热点PD-1单抗。
根据合作协议,信达生物和礼来将合作开发、生产和销售上述新药,其中信达生物将合作主导中国市场的开发、生产和销售,礼来将合作主导国外市场。如果以上抗体在国外商业化,信达生物将收到额外的销售提成和其他付款。
除了与礼来的合作,信达生物还与岸迈生物等机构进行共同发现单克隆抗体等合作。信达生物已于2018年登陆香港生物科技板4。
模式二:通过买入大型药厂处于临床中后期的潜力新药在大中华/亚太地区的许可权,更快速地在中国进行后期临床试验及商业化,取得不俗的回报。
再鼎医药
再鼎医药与制药公司的合作模式是通过支付授权费 ,取得研发后期产品在大中华地区或亚太地区的研发和代理权 。根据公开信息 ,从2014年以来,再鼎医药先后分别从赛诺菲、BMS、Tesaro等药企获得大中华地区研发及销售授权,再鼎医药以此建立起其管线产品5。
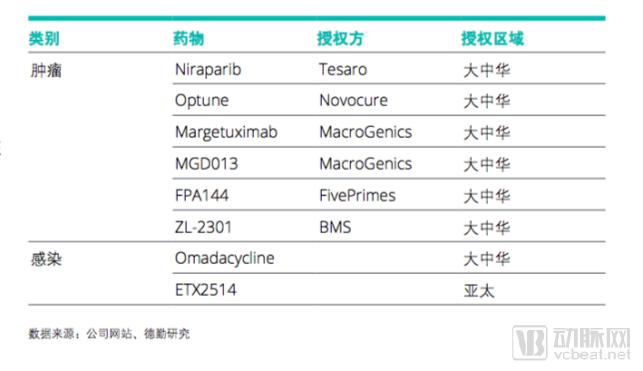
模式三:完成临床II期试验并开展III期试验时,药企通常已投入大量资金及时间并获得了宝贵的试验样本数据。创新型生物科技公司通过获取在临床试验III期中未达效果的新药权利,基于其独占技术可以以较低的成本对药物进行重新开发,研发周期得以节约,从而保证公司获得长期丰厚回报。
索元生物
索元生物与大型药厂合作的模式是,收购大型药厂研发阶段较为靠后的拥有全球权力的在研管线,基于人工智能与大数据的生物标记物平台,精确地寻找与药物疗效相关的生物标记物,并针对敏感人群完成新药的研发。
根据公开信息,索元生物分别从礼来公司、BMS等购得了三款首创新药的全球全部权利,其中一款为处于临床III期的小分子抗肿瘤药Enzastaurin,索元生物去的了该药全球开发、生产和销售的全部权利以及所有的知识产权和其他权利与信息,开展了一系列包括弥漫性大B细胞淋巴瘤(DLBCL)和脑胶质瘤(GBM)的III期临床试验。另一款为礼来公司已完成临床II期试验的抗精神分裂症首创药Pomaglumetad,索元生物取得了其全球所有报批材料、临床数据、专利及商标权利,预计近期将展开III期临床试验。索元还从BMS和AMRI取得了用于治疗耐药性抑郁症的首创新药Liafensine的全球权利,拥有该要在全球的研发、生产及销售权利6。
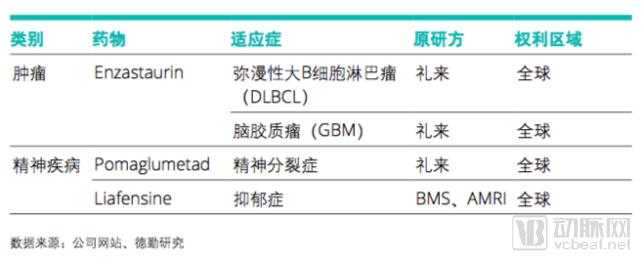
模式四:专业团队基于早期在大型知名研究机构的研发成果,从无到有进行首创新药的自主研发
心悦生医
心悦生医的专业团队由拥有丰富从业经验的资深人士组成,基于其早期在大型知名研究机构或学术中心积累的药物研发成果,自主研发治疗中枢神经系统相关疾病的全新种类药物。
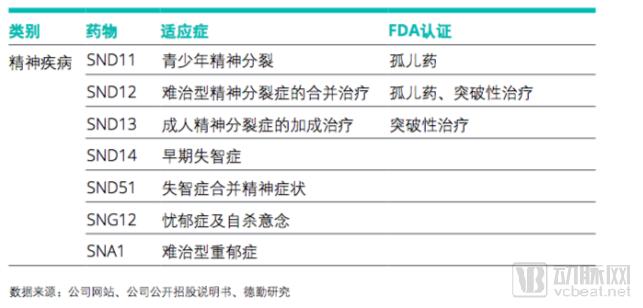
根据心悦生医公开招股说明书所示,其研发管线的知识产权由创始人在早期所属的知名研究中心(麻省总医院及加州大学洛杉矶分校)时发明,多项在研药物已获得FDA罕见疾病药物(孤儿药)、突破性治疗认证。其中,孤儿药的独占权将长达7-7.5年。
研发完成或取得阶段性突破后,心悦生医将通过与国际大药厂的合作及授权,获得高价值的首付款、里程碑付款及上市销售后的收入分成7。
尾注
1. IQVIA Market Prognosis, Sep 2018.
2. Deloitte uk measuring return on pharma innovation report 2018.
3. IQVIA Market Prognosis, Sep 2018.
4. 信达生物招股书
5. 再鼎医药公司网站:http://www.zailaboratory.com/
6. 索元生物公司网站:http://www.denovobiopharma.com/Chinese/
7. 心悦生医公司网站:http://www.syneurx.com/
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。