
# 热门搜索 #
单细胞仪器首证!浚惠生物单细胞图像分析自动分离仪成功取得二类证
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持2020年5月21日,NMPA官网上显示,浚惠生物的单细胞图像分析自动分离仪,经湖南省药品监督管理局批准,正式取得第二类医疗器械产品注册证。

单细胞图像分析自动分离仪
这是目前为止国内批准的第一款临床级应用的单细胞图像分选设备。此前无论是国产还是进口,都没有同类产品获得过药监局的批准进入临床应用,这也意味着单细胞测序打开了临床市场的大门。
本该是一件震动液体活检行业的大事,作为当事人的浚惠生物却对此显得意外的低调。或许在他们眼中,产品最终成功拿证可能更像是水到渠成的一件事情,是他们四年来努力研发的必然成果。另一方面或许也因为,今年的浚惠生物还有几件马上要发生的大事。
CTC和ctDNA是肿瘤液体活检的两大主要方向。近两年,从研究的热度上,ctDNA的风头逐渐有些盖过了CTC。但从理论上讲,CTC涵盖了肿瘤基因组、转录组和蛋白质组的全部信息,理应比ctDNA的内容更丰富。会被ctDNA盖过风头,侧面说明CTC的价值,还没能被完全挖掘出来。
学术界近年来认为,单细胞测序可能会成为打破CTC研究瓶颈的关键技术,并因此在临床上广泛应用。被称为CTC之父的德国汉堡大学的Klaus Pantel教授,2019年8月在《Nature Reviews Cancer》上发表的名为《通过循环肿瘤细胞的单细胞分析揭示肿瘤异质性(译)》的综述文章,也认为单细胞技术可以实现CTC的全面检测,并终将揭示肿瘤治疗中的转移和抵抗机制。
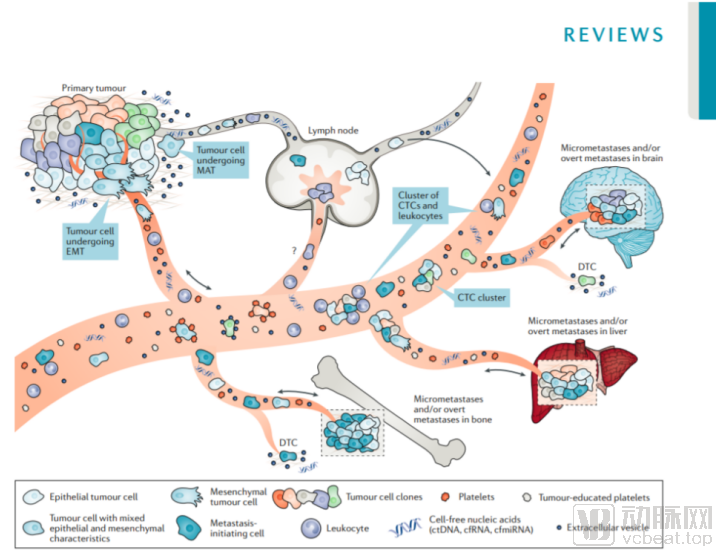
与CTC相关的研究成果示意图
然而单细胞测序在CTC领域的应用,却存在“卡脖子”的技术瓶颈,难以进入临床。
“CTC领域一直以来面临着两个比较大的技术瓶颈,一是缺乏有效的标志物,二是由于数量太少,需要采取单细胞测序的方法获得基因信息,但却一直无法在临床水平上实现。”浚惠生物创始人阎灼辉告诉动脉网。
全球范围内已经有些CTC相关的检测平台。其中最知名的,无疑是CellSearch。
2011年,CellSearch获得CFDA(现NMPA)批准的第三类医疗器械注册证,正式进入国内临床市场。其相应的检测试剂盒和质控品,也都申报通过了三类证。然而到2015年注册到期时,强生却没有选择重新注册,而且在几年后将CellSearch出售给了意大利药企Menarini,战略性放弃了这一产品。
被战略性放弃,问题的根源还是要到系统自身上去找。CellSearch System使用的上皮细胞标志物,在乳腺癌上表现比较好,但在更多的其他癌种中,表现有些不尽如人意。另一方面,系统在临床上的应用也仅限于CTC计数,并不包括分离和测序,并且其中有大量的阳性细胞并不是肿瘤细胞。换言之,本段最开始我们提到的两大CTC领域的瓶颈,CellSearch都没能很好的解决。
瓶颈是痛点,也同时意味着机会。而这个机会,浚惠生物抓住了。
2017年,浚惠生物的首席科学顾问,复旦大学生物医学研究院的施奇惠研究员,在《PNAS(美国科学院院刊)》上发文,提出和PET-CT相同检测原理的葡萄糖代谢标志物可以很好的鉴别出CTC,突破了原本CTC检测缺乏标志物的瓶颈。
这项研究和相关的多项专利直接奠定了浚惠生物的技术基础。由于葡萄糖代谢标志物已经成功应用于临床PET-CT检测,并且结合单细胞测序的能力,浚惠生物将自己的产品平台称为“单细胞seq-PET”。
在此基础上,浚惠生物在对该成果进行临床转化的过程中,在2015年底总结出了CTC单细胞测序进入临床的三大产品瓶颈。
第一是效率问题,每个细胞样本需要一个人看两天,手工挑选出其中的CTC单细胞,再进行单细胞建库测序,整个检测流程非常长;第二是成本问题,过长的时间流程消耗的人力成本,加上当时本来成本就比较高的单细胞基因组测序,让仍处于发展早期的浚惠生物有些吃不消;第三,就是生物标志物问题,当时的葡萄糖类似物检测需要经过细胞培养过程,这样一来对细胞的活性要求很高,而样本在经过采集和运输之后,细胞活性不免要下降。
于是在接下来的四年多时间中,浚惠生物开始着力解决这三方面的问题,同时准备推进自己产品的报证工作。
应对效率问题,浚惠生物组建了自己的软件团队,开发了自动识别细胞的软件。目前已经可以实现5分钟完成一个样本的识别工作,与此前的2天时间相比,大大提高了识别效率。而单细胞的自动分离,更是把手工分选的时间从1天分离20几个细胞,到几秒钟分离1个细胞,效率提高几百倍。
应对成本问题,浚惠生物实现了高效率的单细胞基因片段靶向扩增,优化了WGA单细胞扩增试剂,这样在进行靶向突变基因和CNV的检测时,只要几个细胞就可以完成相关的检测,大幅降低了成本。
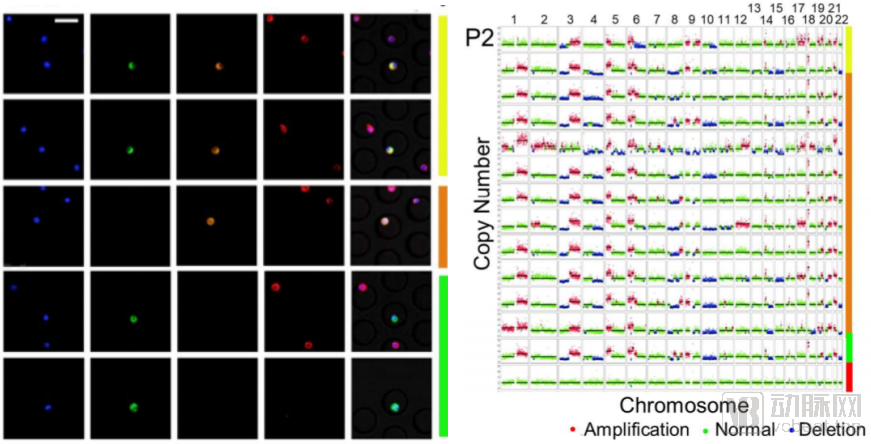
浚惠生物的单细胞“seq-PET”检测
应对标志物问题,浚惠生物找到了参与葡萄糖代谢相关的新的特异性标志物。这样一来,分选之前不再需要培养过程。新方法使用经固定的样品就可以完成后续检测过程。这一新的分子标志物又经过了大量的临床验证过程,仅在泌尿肿瘤上的研究,就纳入了800多例健康人和700多例膀胱癌患者,检测结果和临床的一致性接近90%。尤其在疑难杂症的确诊上,已经体现出了非常高的临床应用价值。
于是2017年,做好了一切准备的浚惠生物,开始向报证发起冲击。
“因为我们是第一个吃螃蟹的人,没有现行的标准依据,所以报证环节不免会遇到些困难。”阎灼辉说。
在报证阶段,因为是第一个单细胞图像分析和自动分离的产品,浚惠生物2018年首先经过省局、国家局的分类界定,确定了产品类别和名称;2019年进行了240多人的多中心临床试验。该项试验的主要结果,经染色的单细胞阳性细胞判读结果,与显微镜下人工观察的结果,一致率可达98.1%;目标单细胞的分离和回收的效果非常喜人,分离成功率达98.2%。
进入2020年,在疫情状态下,为了支持医疗器械创新,湖南省药监局、评审中心组织专家,疫情期间召开网络专家会议,在严格按照法规审核、不降低标准、并落实注册人制度的前提下,用时五个月完成了对浚惠生物“单细胞图像分析自动分离仪”的审批。最终在2020年的新冠疫情期间,浚惠生物获得首个临床用途的单细胞自动分离II类医疗器械注册证。
《Nature》2017年7月曾出版过一期单细胞专刊,其中的综述文章做出了一个大胆的预测:十年内,血液样品或其他活检样品的单细胞检测将成为常态。

《Nature》单细胞专刊
目前,单细胞测序还只被广泛认为是科研级技术,离临床还很远。但是,浚惠生物的团队却认为,临床应用近在咫尺:“液体活检+单细胞测序进入临床,是必然可以近期突破的临床应用。”
看好单细胞测序进入临床的巨大潜力,以及对浚惠生物的发展成长的看好。浚惠生物的早期投资方,专注医疗健康领域创业、孵化的贝壳社的联合创始人范志强,2019年底全职加入浚惠生物,负责产品的市场营销和临床推广。
范志强提到,全球已经有越来越多的企业,在肿瘤单细胞测序的临床应用上开始发力:“比如Epic Science的CTC前列腺癌ARV-7伴随诊断,可以对接单细胞挑取,进行临床样本的单细胞测序; 另一家企业,RareCyte则开发了用于CTC单细胞测序的稀有单细胞自动分离系统,并参与了礼来新药开发的伴随诊断。浚惠生物与全球走在最前沿的肿瘤单细胞测序企业在同一起跑线,我们希望浚惠加快发展,可以在全球领跑。”
浚惠生物本次报证的单细胞分离平台,是浚惠生物开展单细胞临床应用的重要基础。仅在辅助诊断方面,根据尿液、多种体液、血液和宫颈粘液四类不同的样品,就已经形成了这一平台的四大应用场景。
尿液检测膀胱癌的uro-PET产品已经优化的比较完善,先对肿瘤细胞进行鉴定分离,随后再进一步对分离的肿瘤单细胞进行测序。首个膀胱肿瘤细胞检测使用的配套试剂,也已经获得了相关注册证,为后续多种体液样本、多种肿瘤单细胞检测的应用,奠定了进入临床的基础。
目前膀胱癌的诊断方法主要通过膀胱镜,有创而且痛苦,依从性差。浚惠生物的产品和临床上使用膀胱镜的诊断方法一致性接近90%,未来有机会为更多健康人提供膀胱癌筛查,开启“滴尿验癌”新时代。
浚惠生物2020年4月在福建的一个疑难病例的检测上,范志强从医院拿到尿液样本,交给实验室进行检测,很短的时间里,帮助为一位9个月不能确诊的患者实现了确诊,临床医生对于uro-PET单细胞的应用充满肯定和惊喜;在江苏省一家医院的检测中,一个月内发现了三例常规临床手段未确诊,但uro-PET单细胞检测阳性的病例,其中一例较常规检测提前2个月确认了癌症,其他两例也在持续随访中。“2020年将把浚惠seq-PET系统推广到更多的医院,让中国原创的新技术更多的被医生和患者接受”,范志强充满信心。
体液检测的试剂盒也已经完成了体外诊断试剂备案,覆盖多癌种,主要针对胸水、腹水、脑脊液等样本,覆盖包括肺癌、乳腺癌、结直肠癌、淋巴癌等多癌种的检测,可以明显提升细胞病理医生鉴别胸水、腹水、脑脊液等体液中肿瘤细胞的灵敏度。浚惠生物的PET-CT类似标记物和单细胞图像分析仪器,不依赖于形态学鉴别肿瘤细胞,并且实现检测流程中的全自动,解决了目前细胞学检查中灵敏度有限、专业人员缺乏的问题,是解决临床痛点的重要技术革新。
血液CTC检测主要用于肿瘤转移的早期监测,结合肿瘤细胞的分子和生物学特征进行针对性治疗和控制,大大减少因肿瘤转移导致的死亡。从阎灼辉的角度看来,多癌种血液CTC单细胞检测产品的研发已经到了最后阶段:“已经获得注册证的平台,完全可以尽快应用到血液上。我们接下来的主要工作,就是再通过进一步的临床验证,完成CTC检测试剂开发,报证。然后就可以推到临床阶段,为患者服务了。”
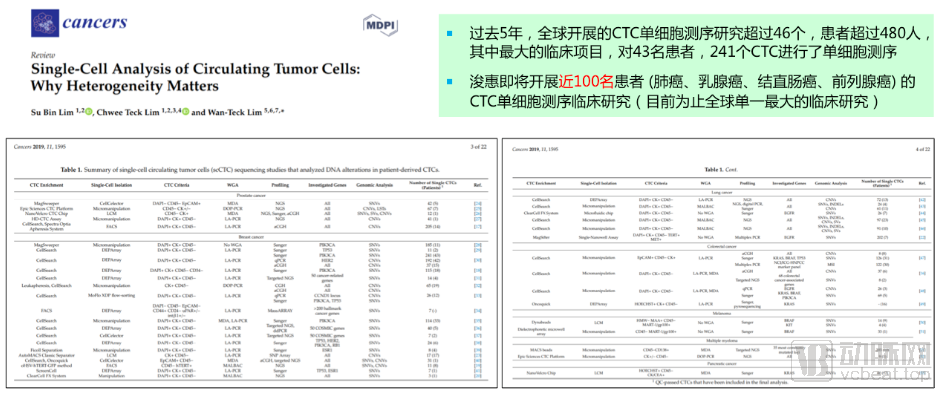
即将开展的血液CTC单细胞相关研究,或将成为全球单一最大临床研究
在血液中的相关研究也将很快启动。浚惠生物预计将在今年内将开启一项入组人数约100人的预实验,来验证自己的血液检测产品。100人的试验规模可能在大多数领域都不算大。但是肿瘤CTC单细胞测序领域,已经几乎是目前为止全球最大的临床试验规模了。
浚惠生物的单细胞诊断平台,还可以从女性宫颈粘液中捕获到胎儿单细胞,进行无创产前筛查(NIPT)。目前基于血液的NIPT产品,仅限于几种染色体遗传病的检测。而胎儿单细胞携带所有遗传信息,可以开展数千种遗传病的筛查。因此把现有的NIPT提升到单细胞Cell-based NIPT,具有巨大的临床意义。
除了辅助诊断之外,平台的价值还将继续向新药研发与伴随诊断的方向拓展。
2019年,施奇惠课题组又和另外两个课题组合作,在《Nature Communications》上发文,继续延伸这一研究成果。新的研究中发展了一种基于液体活检的肿瘤单细胞代谢分型的方法,能够预测对靶向治疗或化疗无效或只能短期获益的患者。
目前,浚惠生物已经开始针对肺癌的PD-L1/PD-1药物,做基于CTC单细胞测序的伴随诊断和疗效监测的研究。
对于诊断之后的创新药疗效监测、与药企合作的新型伴随诊断标志物开发、在美国FDA的注册申报工作等,浚惠生物将会逐渐提上日程。期望发挥液体活检、和单细胞测序的价值,帮助解决更多临床的难题。
浚惠生物也在产品研发之外,做了更多国际一流专家的学术交流。在团队的不懈努力下,2020年的国际液体活检大会被引入中国,落地上海,并很荣幸的成为首个钻石赞助商。虽然由于疫情的缘故,原定线下的会议被调整为了线上召开。但这丝毫不影响这一会议的含金量。CTC之父Klaus Pantel教授、MSKCC的Howard Scher 教授, NIPT之父卢煜明教授、陆舜教授、吴一龙教授、汤富酬教授等都已经确认出席今年的会议。每一位专家都是全球液体活检领域的巨星。“浚惠生物能够支持这样的全球KOL与中国临床、科研、产业界的交流,我们倍感荣耀。”范志强说。

2020国际液体活检大会
“创业之前,我曾经做过一个项目,准备把一家英国企业的技术转移到中国来,然而进展非常不顺利,推进中遇到了很多的问题。在那个项目中我就体会到,虽然全球技术整合是大趋势,但是根本上的问题在于国内企业的创新和技术能力的不足,会导致没办法把好的理念落实到应用当中。没有自主的创新,就不可能整合领先的技术,也得不到国际伙伴的尊重”阎灼辉说。
这也成为了浚惠生物对创新技术研究、临床转化的执着。在过去的几年中,浚惠生物一直在专注于自己的产品技术研发,与临床和学术界进行持续的沟通,不断的打磨自己的产品,并最终将成果成功的投入了市场。
在接下来一系列大动作的面前,刚刚完成报证的浚惠生物根本来不及庆祝。CTC单细胞测序领域,正赶上最好的发展时机,浚惠生物,也正处于把肿瘤单细胞测序平台seq-PET推入临床的、最好的发展状态。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。