微生物疗法是近几年发展起来的新兴生物医药赛道,发展迅速。2015年全球只有少数几个药物在研,到现在涉足微生物疗法的企业有上百家,全球在研管线数百个。2020年8月,Seres Therapeutics公布了肠道微生物疗法SER-109治疗艰难梭菌感染的三期临床阳性结果,引发了行业极大关注。资本端也对微生物疗法赛道寄予厚望,百亿美金持续押注1。2015年,Seres Therapeutics成为首家在纳斯达克上市的微生物疗法企业;2020年9 月,Finch Therapeutics完成 9000 万美元 D 轮融资;2021年1月,Vedanta Biosciences获得辉瑞领投的2500万美元投资;2021年3月,Finch Therapeutics成功在纳斯达克上市,开盘大涨30%。
最近十年,全球微生物疗法的专利数量也呈井喷式增长,其专利保护以发现新的微生物菌种及其药效功能为基础。法国LNC Therapeutics公司在2019年引进了康奈尔大学关于肠道细菌Christensenella minuta在减肥适应症的专利,目前正在开发基于Christensenella minuta的减肥和代谢疾病的药物。而英国4D Pharma公司2018年在美国获得授权的专利保护了一个重要的肠道细菌属Bacteroides在整个治疗领域的应用。截止至2020年底,全球报道发现的肠道细菌可培养物种一共仅为1332种2,其中新物种为307种3,如何快速专利、开发新的肠道细菌物种及其功能,成为全球微生物药物公司的军备竞赛。
作为国内领先的微生物疗法企业,慕恩生物已经完成3轮融资,投资方均为国内一线生物医药投资机构。慕恩生物目前已经发现、保存、鉴定肠道细菌物种1104个,新物种为318种,新物种数量比全球其他机构的总和还要多,建立了超过14万株的全球极具竞争力的微生物菌种库。公司依托领先的全谱活菌药物开发平台,瞄准微生物疗法在肿瘤免疫和代谢疾病领域的治疗潜力,正在进行多个药物管线研发,旗下针对肿瘤免疫和代谢疾病的两个管线,今年有望成为国内该领域首个进入临床的活菌药物(Live Biotherapeutic Products, LBPs)。
慕恩生物创始人兼CEO蒋先芝博士表示,慕恩生物自成立之初就定位于平台型的微生物组技术公司,致力于搭建起从发现微生物(发现、培养新的微生物多样性)、筛选微生物(通过数据和体外、体内筛选模型高通量筛选目标功能菌株)、改造微生物(通过人工进化和合成生物学技术改造微生物的性状)和应用微生物(基于高效发酵优化、制剂技术和应用测试,开发不同应用场景的微生物产品满足市场需求)的完整微生物组产业化技术体系。在生物医药板块,慕恩生物已经成功打造了一个全谱活菌药物开发平台,建立了符合GMP的生产设施,可同时推进多个研发管线,不断扩展适应症,降低成本,有效加快药物研发速度。“基于全谱活菌药物开发平台,慕恩生物能够把微生物药物从Discovery到进入临床的时间控制在1年半左右。”蒋先芝博士这样说到。
目前,慕恩生物拥有9个研发管线。与大多数企业拥挤在CDI和IBD适应症赛道上不同的是,慕恩生物是少有的覆盖肿瘤免疫和代谢性疾病两大适应症的企业。

▲慕恩生物活菌药物管线图 | 图源:慕恩生物
谈及适应症选择策略,蒋先芝博士如此说:“肠道菌群被认为与多种疾病相关,但是这种因果联系有的紧密、有的松散。我们首先考虑的是哪种适应症与肠道菌群有更强的关联性与因果关系,可以起到更好的治疗作用4-10。已经有大量研究表明肠道菌群会影响肿瘤免疫和代谢疾病治疗效果。其次,从临床需求看,全球仍然有着大量肿瘤和代谢疾病患者缺乏好的治疗方案,市场规模达2000亿美元。最后,从全球竞争格局来看,肿瘤免疫和代谢疾病领域的研发进度差距不大,未来中国很有可能在这两大细分赛道上诞生微生物疗法全球独角兽。”
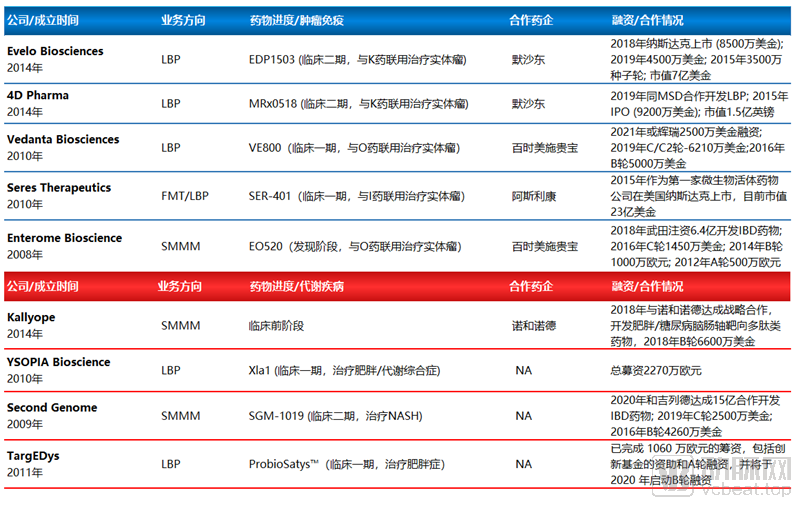
▲药物开发进展:跨国医药公司通过合作进入微生物治疗,国外多个项目进入临床
数据来源:各企业官网,慕恩生物整理
MNC-168和MNO-863是慕恩生物在肿瘤免疫和代谢疾病领域布局的两大重磅研发管线,预计今年内进入临床。
MNC-168是慕恩生物原创且受全球专利保护的一种创新肿瘤免疫活菌药物。透过所搭建的低应答冷肿瘤模型显示,MNC-168在多种肿瘤的单用疗效上,抑瘤率均显著超越PD-1,最高可达近60%的抑瘤率及肿瘤完全消失。更为重要的是,MNC-168与PD-1免疫检查点抑制剂联用时(不限肿瘤),抑瘤率最高可达近90%,并且显著将冷肿瘤PD-1应答率从0-37.5%提升至80-100%,其临床前药效媲美甚至超越目前的主要活菌药物赛道对手-4D Pharma (MRx0518)、Evelo (EDP1503)、Vedanta (VE800)、Seres (SER-401)及Genome & Company (GEN001)的临床在研药物单用或同PD-1抑制剂联用的抑瘤率 (单用: 0-55% 联用: 70-80%)。
凭借其创新多靶向肿瘤免疫激活与微环境调节的作用机理,MNC-168未来将具备高度临床治疗潜力应用于解决难治型肿瘤患者及70-80%的PD-1未应答族群的未满足医疗需求,将可赋予其渗透并抢占超过700亿美金肿瘤免疫市场。
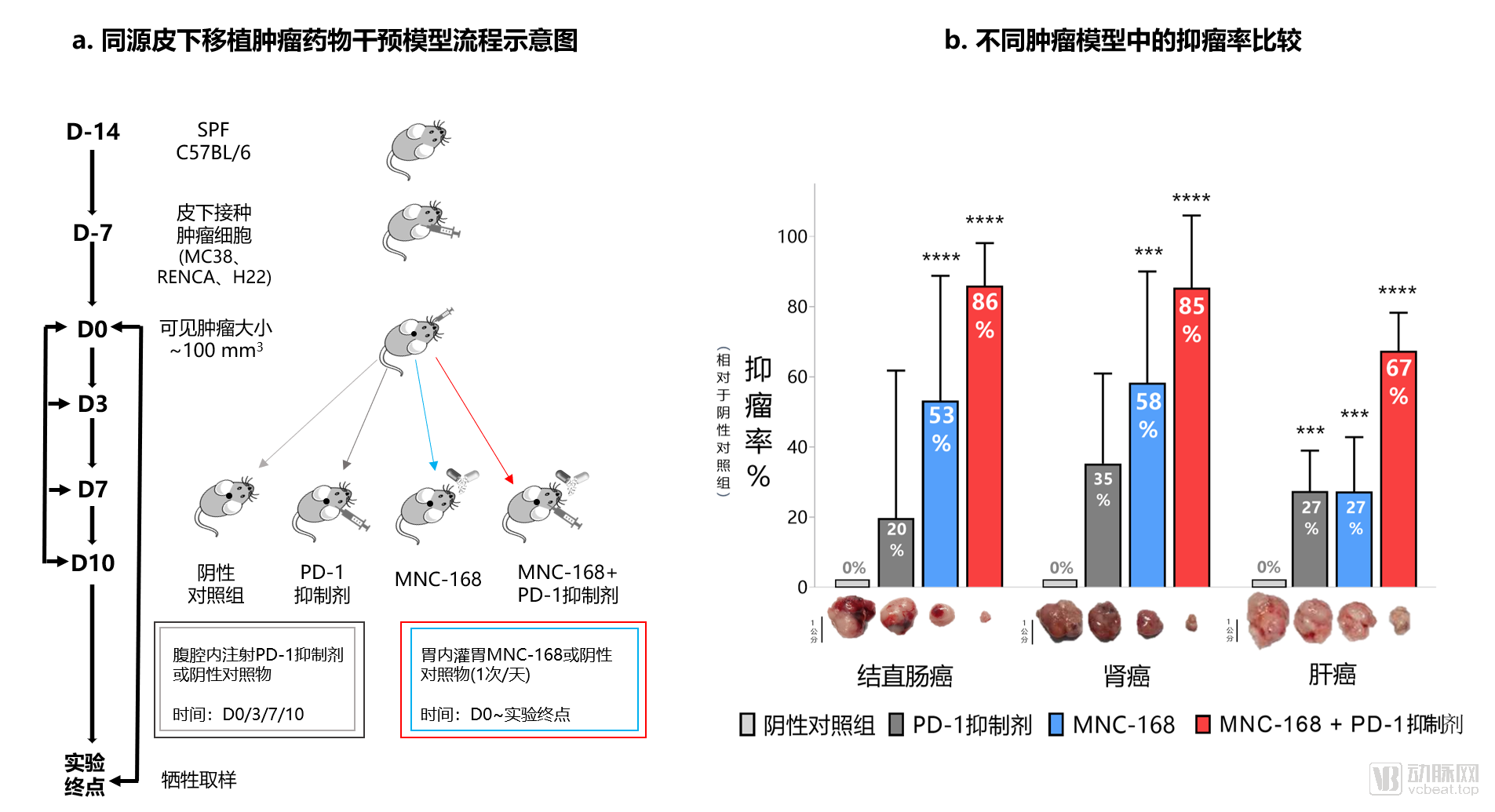
▲MNC-168具备多种肿瘤单药及与PD-1抑制剂联用疗效 | 图源:慕恩生物
MNO-863是由慕恩生物原创且受全球专利保护的一种创新性代谢疾病活菌药物,用于治疗肥胖症/代谢综合症与相关代谢异常疾病。透过典型治疗性高脂肥胖小鼠模型显示,MNO-863单药干预四周即可降低体重近10%,其减重药效可媲美现今一线非处方减肥药物奥利司他及已上市的GLP-1R激动剂减肥药物,同时还具有20-43%体内脂肪下降、14-26%高血脂指标下降(甘油三脂、总胆固醇与低密度脂蛋白),且与此GLP-1R激动剂减肥药物联用下平均可超过20%的减重效果,更重要的是,MNO-863在停药后仍可减缓复胖的问题,具备高度改善现有药物痛点的潜力。
此外,进一步的临床前药效结果指出MNO-863更可显著逆转二型糖尿病及非酒精性脂肪肝炎的关键指标,包括 30%空腹血糖下降、葡萄糖耐受性改善及显著降低非酒精性脂肪肝病病理指标(NAFLD activity score)至2分。
MNO-863的临床前药效均超越现有肠道靶向赛道对手-TargEDys (ProbioSatysTM)、Second Genome (SGM-1019)、YSOPIA Biosciences(Xla1,原LNC01)、Kintai (KTX0200)的在研药物的疗效,透过其创新多靶向糖脂代谢调节、能量燃烧及肠道障蔽能力作用机理、高度安全与药物协同作用之特性,将可赋予其渗透与抢占超过1000亿美金的代谢疾病单用与联用的巨大市场。
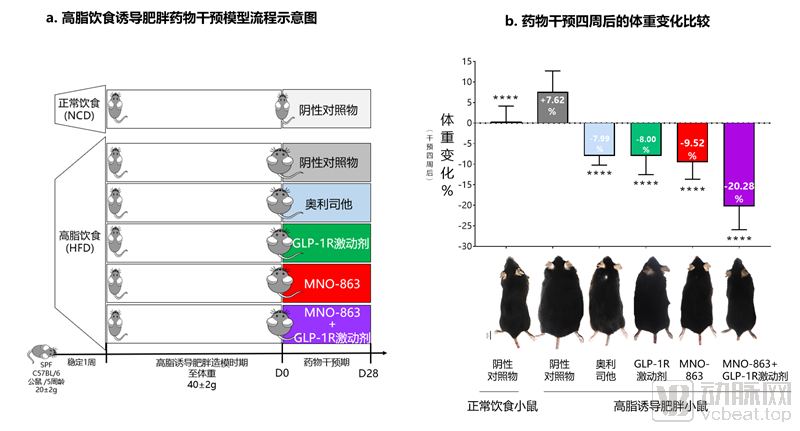
▲MNO-863媲美一线减肥药物:单药10%及与GLP-1R激动剂联用超20%减重疗效 | 图源:慕恩生物
值得注意的是,MNC-168和MNO-863即将在中美两国申报IND,有望成为国内在该领域首个进入临床的药物,2021年慕恩生物也将成为临床阶段的微生物疗法生物医药公司。
需要明晰的是,一个完整的微生物药物开发流程包括“微生物发现-功能筛选、功能鉴定-成药性评价-临床应用”。菌种资源发现是微生物疗法的源头,也是必经之路,往往需要以最严格的知识产权手段予以保护。可以说,新菌种、新菌株的开发是微生物组产业的“芯片”。
在欧美,越来越多的微生物疗法企业将他们的菌株以专利家族的形式公开保护,专利范围可以覆盖对应的细菌物种及其应用。以4D Pharma为例,旗下的人罗斯拜瑞氏菌Roseburia hominis(主要适应症为溃疡性结肠炎),专利授权覆盖了美欧日韩澳大利亚等多个国家和地区;另一株主要应用于IBS的Blautia菌株专利申请,更是从种属层面向下覆盖至各种适应症。截止至2021年3月,4D Pharma总计公开了近1000件专利,超过100件同族,专利进入了多个国家和地区,覆盖了其所有研发管线。
如何快速专利、开发新的肠道细菌物种及其功能,已成为全球微生物药物公司的军备竞赛。
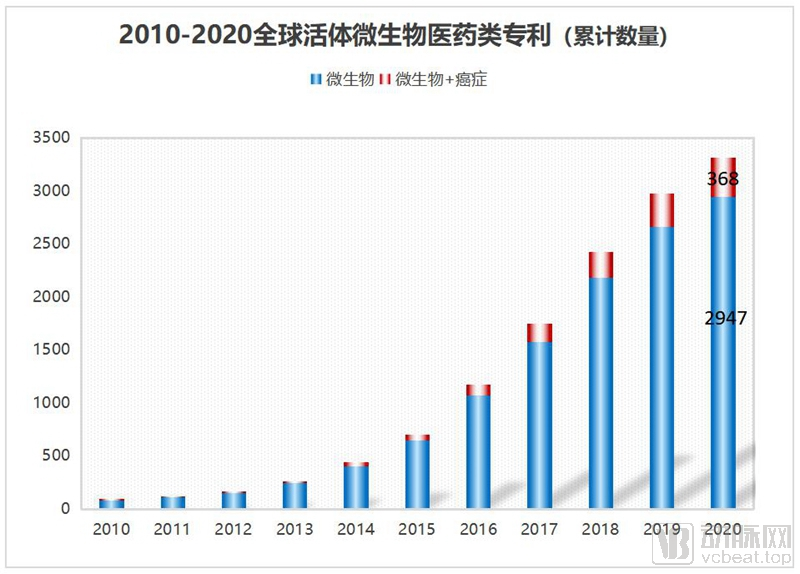
▲最近十年,全球微生物疗法的专利数量呈井喷式增长 | 图源:慕恩生物
近年来,随着宏基因组技术的发展,大量未培养肠道细菌信息得以发现,但技术本身存在“深度偏差”等缺点亟待解决。2012 年Lagier JC等提出微生物培养组学 (Culturomics)这一概念后,在一定程度上减小了宏基因组学的误差,设计、优化多样化的培养条件和营养成分,极大提高了培养效率,结合MALDI-TOF质谱和16S rRNA测序等技术,使得可培养的人体细菌增加了几百种,很多新菌种也通过培养组学方法被发现。
尽管如此,目前被发现的肠道微生物仅有1000多种,已知肠道微生物的种类有限,具有开发价值的肠道微生物更是稀少。“也就是说,越到后面发现新菌种的可能性越来越小,难度也越来越大。新菌种的发现及其应用就是国与国之间,也是企业与企业之间的军备竞赛。企业拥有的新菌种越多并快速进行专利保护,护城河也就越深。”蒋先芝博士谈到。“我们不能等到数年之后,大多数的肠道细菌的应用都被其他国家的公司专利保护了,我们吃自己肠道的细菌都要给国外公司付专利费,那时就追悔莫及了。”
中国幅员辽阔,人口众多,人们的饮食习惯、遗传背景差异大,人群多样性非常高,且样本获取成本也更低,“与国外比,中国在新菌种及其功能发现上具有得天独厚的优势。” 蒋先芝博士表示。国内目前有多家公益性的菌种保藏机构,但在企业端,由于中国具备生物勘探能力、培养组学创新能力、微生物产业化背景的团队非常稀缺,所以国内的微生物疗法企业大都不会涉足新菌种发现和新菌种功能的专利保护这一领域,往往是通过购买外部菌种专利或者在国内申请保护范围极窄的菌株专利的方式进行药物开发。
作为国内少有的平台型微生物组的创新公司,慕恩生物一直致力于把领先培养组学技术和新菌种、新菌株功能的高通量筛选作为核心竞争力,从2015年成立之初就开始构建自有菌种库,投入了大量人力物力精力,将肠道菌群的培养组学做到了极致,可最大限度的分离、培养出有价值的菌种。
现在,慕恩生物已经打造出了一个大规模、多样性的微生物资源发掘中心,保存的菌株超过14万株,其中人体肠道细菌超过6万株。据Nature biotechnology最新文献2统计,截止至2020年底,全球(其他机构)发现肠道细菌可培养物种为1332种,其中新物种为307种;慕恩生物发现肠道细菌可培养物种为1104种,新物种为318种,新物种数量比全球其他机构的总和还要多。
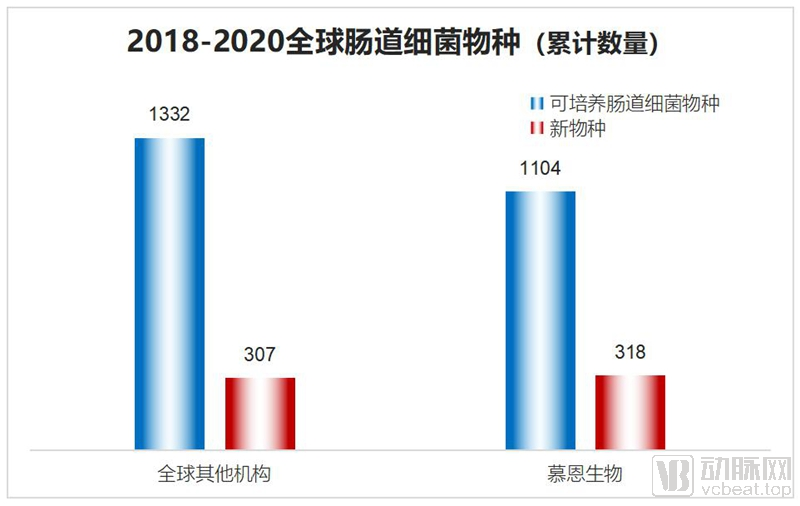
▲慕恩生物VS全球其他机构:可培养肠道细菌物种及新物种数量(2018-2020) | 图源:慕恩生物
值得关注的是,慕恩生物在重要微生物菌株资源挖掘上积累了大量新物种,例如,在Ruminococcaceae菌科和Bacteroides菌属发现并保存了超12个新属,31个新种。这意味着,慕恩生物所掌握的微生物多样性资源在全球都极具竞争力,同时这也是慕恩生物打赢全球微生物疗法军备竞赛的核心武器。
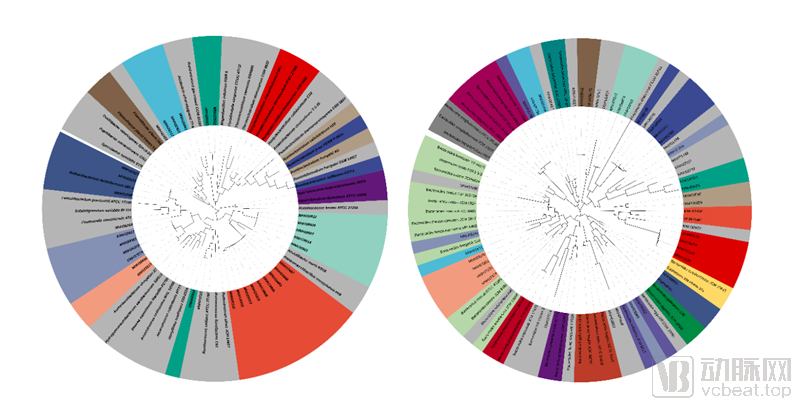
▲慕恩生物在Ruminococcaceae菌科和Bacteroides菌属获得并保存的新属和新种级菌株 | 图源:慕恩生物
微生物疗法是近年生物学研究热点,已经成为新的研究和投资风口。据统计,全球人类微生物组治疗市场预计将以63%的复合年增长率增长,市场空间不断增长。预计2021年将诞生全球首个微生物药物,微生物疗法势必会在最近几年迎来大爆发。
蒋先芝博士认为,微生物疗法领域有四大趋势。一是生物医药行业和投资机构对微生物疗法的认知程度越来越高;二是适应症会不断拓展,从肠道疾病发展到肿瘤免疫、代谢疾病和神经系统疾病等;三是生态圈逐渐完善,上游服务机构越来越多,已经出现专门从事微生物疗法的CRO和CDMO公司;四是对肠道菌群的研究越来越深入,从关联分析、因果联系,发展至分子层面的机制研究。
毫无疑问,慕恩生物选择的是一条极具前景的赛道,乘着行业春风,慕恩生物将扩大样本采集来源,继续丰富菌种库多样性和加速新菌种的功能筛选,积累重要的多组学数据,同时快速推进旗下药物研发管线。“我们有信心打赢全球微生物疗法军备竞赛,让中国企业占据重要一席之地。”
参考资料:
1、Early investments powering the ascent of microbiome therapeutics. Michael Eisenstein. Nature Biopharmadealmakers FEATURE (2020). (DOI: 10.1038/d43747-020-01178-x)
2、A unified catalog of 204,938 reference genomes from the human gut microbiome。Almeida A et al., Nature Biotechnology (2021). (DOI: 10.1038/s41587-020-0603-3)
3、Updating the repertoire of cultured bacteria from the human being. Diakite A, et al., Microbial Pathogenesis (2021). (DOI: 10.1016/j.micpath.2020.104698)
4、The microbiome and human cancer. Sepich-Poore GD et al., Science (2021). (DOI: 10.1126/science.abc4552)
5、Good bacteria make for good cancer therapy. Dart A. Nature Collection Milestones (2020)
6、Fecal microbiota transplant promotes response in immunotherapy-refractory melanoma patients. Baruch EN et al., Science (2021). (DOI: 10.1126/science.abb5920)
7、Fecal microbiota transplant overcomes resistance to anti-PD-1 therapy in melanoma patients. Davar D & Dzutsev AK et al., Science (2021). (DOI: 10.1126/science.abf3363)
8、Gut microbiota from twins discordant for obesity modulate metabolism in mice. Ridaura VK et al., Science (2013). (DOI: 10.1126/science.1241214)
9、Transkingdom interactions between Lactobacilli and hepatic mitochondria attenuate western diet-induced diabetes. Rodrigues RR et al., Nature Communications (2021). (DOI: 10.1038/s41467-020-20313-x)
10、The role of the microbiome in NAFLD and NASH. Kolodziejczyk AA et al., EMBO Mol Med (2019). (DOI: 10.15252/emmm.201809302)








 提供支持
提供支持




















