制药巨头GSK于2017年发布的全球疼痛指数报告显示,全球85%以上的人口都在生活中经受过头痛或者身体疼痛。美国国家科学院统计,美国有超过1亿规模的人群受到持续性疼痛的困扰;在中国,单看患关节炎的患者人群,数量就超过了1亿。
疼痛药市场潜力巨大,在药物销售总金额上,仅次于肿瘤药物和代谢性疾病如糖尿病药物。然而,由于疼痛类药物作用机制复杂、研发难度较大,少有新药获批上市。
近日,被称为“最后一剂治疗骨关节炎的NGF抗体”——Tanezumab(历经15年、41项临床研究,由辉瑞与礼来联合开发的用于治疗骨关节炎的新药)传来消息:
FDA发布文件称,尽管临床试验表明Tanezumab可以帮助骨关节炎患者,但存在着严重的安全问题,并对此表示担忧。而辉瑞、礼来两家公司提出的REMS计划(针对Tanezumab的风险评估和缓解策略)FDA也表示怀疑:因为没有任何数据证明该计划有效。对于是否批准Tanezumab上市,FDA没有当即做出最终的决定。
在多款NGF抗体药物接连被FDA“亮红灯”警报的同时,一家上海初创创新药物研发企业——昌郁医药(Xgene Pharma)研发的疼痛类新药品种XG005却受到FDA“绿灯关照”,与此类事件形成鲜明对比。
去年,昌郁医药XG005-02(口服剂型)获得美国FDA的 “加速通道”资格,由临床I期直接进入III期的关键性临床试验(Pivotal Trial),并有望获得治疗全面急性疼痛上市的新药注册。
近日,昌郁医药再度传来好消息:公司核心品种之一,XG005-03(透皮剂型)于澳大利亚顺利完成I期临床试验,将于近期争取在美国开展临床II期试验。
同样在疼痛药领域,历经15年、41项临床研究,超23亿美金投入,由辉瑞、礼来两大制药巨头联合开发的用于治疗骨关节炎的新药Tanezumab目前的上市前景尚扑朔迷离,而昌郁医药有何特别之处,甚至让审查程序极为严苛的FDA为其开启“绿灯”优待?
作为一家专注于开发治疗神经类和疼痛疾病小分子创新药公司(start-up),昌郁医药旨在利用已上市产品的临床研究新发现,针对市场的需求,重新定位和开发相应的产品,以满足全球众多疼痛患者普遍未得到的临床需求。
昌郁医药利用其特有的“双效”药物偶联研发平台,将具有机制互补或协同作用的药物,进行合理的配对偶联,开发出具有临床疗效并兼备安全性更好的产品。
“双效”药物研发平台是昌郁医药团队在新药研发道路上快速取得成果的秘诀,也是该公司区别于其它新药研发企业的核心竞争力所在,具有研发风险小、开发速度快和市场确定性高等特点,这些优势已在目前开发阶段部分得到证实。
据昌郁医药联合创始人兼CEO徐景宏博士介绍,公司的首发产品XG005是对治疗疼痛的一线用药非甾体抗炎类药物和神经镇痛药物偶联而成,由于两种药物已在临床使用,其优缺点非常清晰,通过偶联所得到的全新分子具有其改良后的化学性质、生化及药代性质,因此,偶联产品具备更好的临床治疗优势。
就昌郁医药的首发产品XG005而言,该款药物不仅能同时治疗炎性和神经并存的疼痛,同时还大大降低了两类药物单独服用或联合服用时所不可避免的胃肠道及中枢神经副作用。与此同时,由于通过偶联平台研发而得的分子为全新化合物,具有其独特的药学特性,因此可以获得全新的化合物专利,产品的知识产权可以得到充分的保护。此外,还可以在原药所有的适应症基础上扩大适应症,以及改变给药途径,增加药物临床使用的方便性和范围。
目前,偶联药物XG005-02(口服剂型)将在2021年进入美国临床III期急性疼痛研究,同时也会于今年上半年申报中国的临床药代桥接研究,加快其在国内上市的步伐。徐博士表示,昌郁医药未来在开发国际市场的同时,也会争取尽早为国内广大关节炎和肿瘤疼痛患者提供疗效明显、安全性优越的产品。
在此套特色新药开发逻辑的背后,是实力强劲的昌郁医药创始管理团队。该团队成员不仅身披顶级名校光环,药物研发及行业经验也十分丰富。
联合创始人兼CEO徐景宏博士是国际知名毒理学家,他曾主持超过30个在欧美、亚洲的新药IND申报,其中20多项已经进入临床II/III期,并有一款药物已上市(Taigenxy®)。截至目前,徐博士也发表学术论文40余篇、获5项专利,还曾主编“癌症风险评估”(John Wiley & Sons,Inc.)、“实验动物临床检验指南”(上海科学普及出版社)这两本书籍。
在美国麻省理工 (MIT)获得毒理学博士学位后,徐博士在美国加州大学伯克利分校完成了博士后的工作。在毕业后第一份在美国环保署的工作中,徐博士曾担任环保署毒理药理部部长。此后,徐博士在多家国际制药公司(默沙东、东阳光药业、益诺思、太景生技)担任高管,拥有超20年的行业经验积累。徐博士还曾任美国华人毒理学会理事长,同时也是美国毒理协会的认证专家。
联合创始人兼首席科学官徐锋博士是美国波士顿大学有机化学博士,就读美国哈佛大学博士后时,师从诺贝尔化学奖获得者E.J. Corey教授。徐锋博士曾在美国的Tularik和XenoPort就职并担任多个研发领导职位,参与过10余个新药的研发,临床试验阶段药物2个,其中包括上市药物Horizant®,拥有超20年的行业经验。
两位高管科学家配合默契,各抒所长,所带领的公司团队运作高效,执行力强。短短5年内,昌郁医药团队就将NCE新药开发推进至美国III期临床。
在过去10年里,美国有超过40万起因过量使用阿片类药物导致的死亡,仅2018年就有超过67,000起事件发生。美国疾病控制和预防中心数据显示,每天有超过140名的美国人死于服药过量,其中91%的死者生前都曾有过滥用阿片类药物的病史。
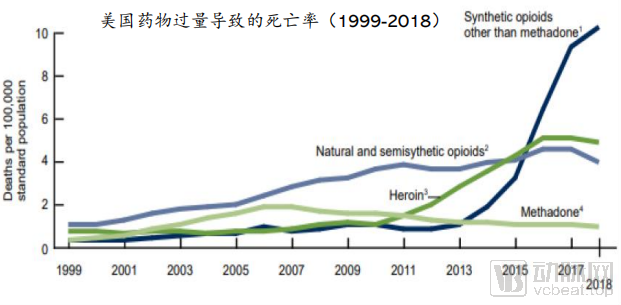
美国1999-2018年因药物过量导致的死亡率(图源:公开资料)
据统计,疼痛治疗领域的“广谱药”阿片类药物所引起的医疗及社会“副作用”每年造成直接及间接经济损失高达800亿美元。
为应对阿片药物成瘾泛滥的问题,欧美各国针对阿片危机采取了一系列严厉管控措施。但全球受到急、慢性疼痛困扰的庞大患者人群却并没有消失。这样一来,疼痛市场上未满足的临床需求就转向了具有相似药效但副作用较少的新型镇痛药物。这样极其特殊的国际局面使得昌郁医药获得了空前的发展契机。
相关市场数据显示,疼痛药市场潜力巨大,是药物销售金额仅次于肿瘤药物和代谢性疾病如糖尿病药物的第三大药物市场。2019年,全球疼痛药市场规模约为606亿美元,急需被替代的阿片类止痛药市场规模则接近200亿美元。因该领域显现的巨大市场潜力,辉瑞、强生、GSK、礼来等制药巨头都在疼痛领域做了积极布局。
近10年来,各级政府对科技创新给予了大力支持,创新生物制药公司像雨后春笋,各类研发模式层出不穷。昌郁医药认为,虽然小药物研发公司在资金、人员方面难以与国际大药企进行竞争,但在“创新模式、开发风险、市场竞争”中探索到一条具备自身特色的创新药研发模式至关重要。
由于极具特色的新药开发逻辑和理念,昌郁医药吸引到了晨兴创投、平安创投、泰福资本、台杉投资等多家投资机构以及印尼金光集团的投资。目前,昌郁医药已经完成A、B两轮融资,累计融资近3000万美元,公司将于近期开启C轮融资。
据徐景宏博士透露,随着临床试验的顺利开展以及一系列可喜实验数据的获得,昌郁医药计划于明年将IPO提上日程。
未来,公司将依托全球团队的高效合作,凭借独特的新药研发模式,开发具有国际竞争力的产品来解决全球镇痛难题,为国内外广大疼痛患者带来福音。








 提供支持
提供支持