
2019年5月12日-2019年5月19日,本周新药数据共17个,其中肿瘤12个,精神疾病、眼科、皮肤、血液及mRNA药物各1个。
❖Amgen公布了KRAS小分子抑制剂AMG510首次人体试验结果。在KRAS相关研发管线中,Amgen此次第一个公布了人体试验数据,较其竞争对手Mirati(2019年1月开始首个KRAS G12C抑制剂临床试验)更胜一筹。随着技术的进步,KRAS等沉睡数十年的靶点都开始慢慢苏醒,预计未来会有更多的进展浮出水面。
❖Iovance公司公布了令人印象深刻的肿瘤浸润淋巴细胞疗法(TIL)的数据。在27名复发性晚期宫颈癌患者中,Iovance治疗的ORR达到了44%,与此同时K药在这一群体的类似试验中ORR为14%。受此利好消息,Iovance股价暴涨40%。
❖2019年ASCO大会将有众多中国肿瘤创新药亮相。根据ASCO年会官网,有638项与中国相关的报告信息(总计4950项)。百济、信达、君实、恒瑞、索元、艾森、倍而达等纷纷将公布最新临床进展,让我们拭目以待。
❖O药屋漏偏逢连夜雨,上周胶质母细胞瘤的3期临床未能达到主要终点,本周日本通报部分使用O药的患者出现下垂体功能障碍副反应危象。11例患者出现下垂体功能障碍,包括1例死亡,疑与Opdivo的使用有因果关系,但具体原因仍有待查明。
Poseida自体CAR-T产品P-BCMA-101
获FDA授予孤儿药称号
FDA近日授予Poseida公司治疗复发难治性多发性骨髓瘤的在研产品P-BCMA-101孤儿药称号。
P-BCMA-101主要由记忆性干细胞样T细胞组成,这种T细胞具有存活久(可存活数十年)、可自我更新、可分化的特征,有助于重建整个T细胞亚群。
1期试验中,23名患者接受了5个剂量组的治疗。目前2期试验在进行中。
1期实验可评估的19名患者中,13名患者达到部分缓解或更优,2名患者达到轻微缓解。2期临床中,患者显示出了100%的ORR。同时,P-BCMA-101显示出了良好的耐受性和安全性。
Amgen旗下在研KRAS G12C小分子抑制剂
首次临床实验取得积极结果
Amgen在ASCO年会上公布了其在研KRAS小分子抑制剂AMG510首次人体试验的积极结果。同时公司计划启动AMG510与抗PD-1疗法联用的临床试验。
AMG510是一种能与G12C突变的KRAS蛋白共价结合的小分子抑制剂。
该项开放标签、多中心、1期临床实验中,22名携带KRAS G12C突变的癌症患者接受了治疗。这些患者此前经过了多种疗法的治疗。
接受评估的10名患者中,2名患者达到部分缓解,6名患者疾病稳定,同时2名患者疾病有恶化情况。
图:AMG510结构
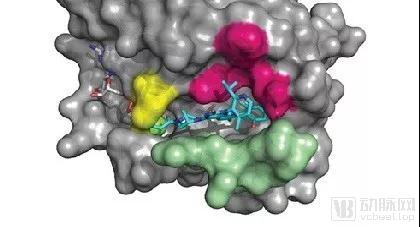
来源:Amgen, ASCO 2019
基因泰克广谱抗癌药Entrectinib
公布治疗脑瘤的积极1期临床结果
基因泰克公布了旗下抗癌药物Entrectinib治疗儿童脑瘤和实体瘤患者的1期临床试验数据。
Entrectinib是一种“广谱”抗癌药物,能够靶向携带NTRK、ROS1或ALK1基因融合的肿瘤,还可穿过血脑屏障。
携带上述基因融合的实体瘤、脑瘤及胶质母细胞瘤儿童患者接受了治疗。
携带基因融合的儿童脑瘤、实体瘤患者在接受Entrectinib治疗后达到了100%(11/11)的缓解率。
Forty Seven公布旗下抗CD47抗体Hu5F9-G4
首次人体临床试验结果
Forty Seven公司将在ASCO公布其在研抗CD47抗体Hu5F9-G4的首次人体临床试验结果,该抗体在本次临床试验中用以治疗急性骨髓性白血病或骨髓增生异常综合征。
Hu5F9-G4(5F9)是一种可抑制CD47的人源化单克隆抗体,能够增强巨噬细胞的吞噬作用并促进T细胞的启动。
15名初治急性骨髓白血病/骨髓增生异常综合征患者接受单药疗法或者阿扎胞苷联用疗法。
15名患者中,8名达到完全缓解,10名复发难治性患者中,1名达到了形态学无白血病状态。并且截至19年1月所有获得缓解的患者都未复发。
信迪利单抗公布信迪利单抗2期临床数据
信达生物在ASCO大会摘要中披露了其抗PD-1产品信迪利单抗治疗复发难治性结外NK/T细胞淋巴瘤的ORIENT-4研究数据。
信迪利单抗是一款国产PD-1单克隆抗肿瘤创新药。
ORIENT-4研究是一项多中心、单臂的2期临床研究, 28名平均接受过3个常规治疗方案的复发或难治性结外NK/T细胞淋巴瘤患者接受了治疗,试验主要终点为客观缓解率。
截至2019年2月,28名患者中ORR为68%,疾病控制率达86%。
君实生物公布特瑞普利单抗
治疗鼻咽癌2期临床研究中期结果
君实生物在ASCO大会摘要中公布了旗下抗PD-1特瑞普利单抗疗难治转移型鼻咽癌的2期临床研究的中期结果。
特瑞普利单抗是一款国产PD-1单克隆抗肿瘤创新药。
本次披露中期数据的是一项开放2期临床试验。
截至今年1月,在135名可评估患者中,客观缓解率为25.2%,疾病控制率为54.8%。
艾伯维与罗氏联合疗法获批一线治疗白血病
FDA批准艾伯维与罗氏共同开发的Venclexta(venetoclax)与Gazyva(obinutuzumab)联用,一线治疗初治慢性淋巴性白血病或小淋巴细胞淋巴瘤患者。
Venetoclax是具有高度特异性的BCL-2抑制剂,能够恢复癌细胞的凋亡。Obinutuzumab是靶向CD20的免疫药物。
批准基于该联合疗法的3期临床研究CLL14。
试验结果表明,与标准疗法相比,该联合疗法能够将患者疾病进展或死亡的风险降低67%。在28个月的随访过程中,87%的患者均没有恶化。
FDA批准辉瑞avelumab与阿西替尼
联合使用一线治疗晚期肾细胞癌
FDA近日批准辉瑞Bavencio(avelumab)与Inlyta(axitinib)联合疗法用于一线治疗晚期肾细胞癌。
该联合疗法结合了PD-L1单抗与VEGFR TKI。
批准基于名为JAVELIN Renal 101的随机、多中心、开放性3期试验。
试验结果显示,联合疗法组显著改善患者PFS(13.8个月VS 8.4个月),同时使得治疗人群的ORR明显提高(51.4% VS 25.7%)。
Iovance肿瘤浸润淋巴细胞疗法
在宫颈癌治疗中表现积极
Iovance公布了其肿瘤浸润淋巴细胞(TIL)疗法LN-145治疗晚期宫颈癌患者2期试验的积极数据。
TIL疗法从患者体内获得肿瘤浸润淋巴细胞,并在体外利用IL-2细胞因子刺激其扩增。之后被激活扩增且提升了抗肿瘤能力的TIL细胞被输回患者体内用于杀伤肿瘤细胞。
接受该疗法治疗的晚期宫颈癌患者此前平均接受过2.6种前期疗法。
27名能够被评估的患者中,1名达到完全缓解,9名达到部分缓解,2名为未确认的部分缓解。综上,该TIL疗法达到了44%的ORR,是K药在类似患者群中的近3倍(14%)。
图:Iovance LN-145疗法22天制备流程
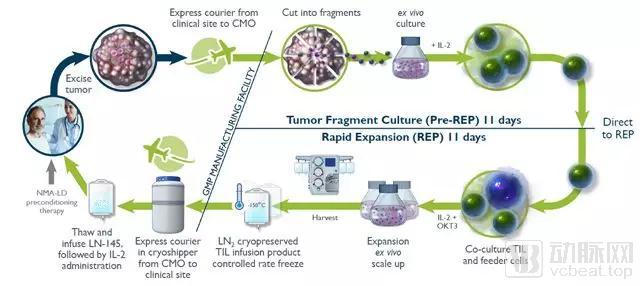
来源:Iovance, ASCO 2018
第一三共新药获FDA投票支持
有望成为腱鞘巨细胞瘤首款获批疗法
FDA药物咨询委员会以12:3的票数支持第一三共开发的新药Pexidartinib用于治疗症状性腱鞘巨细胞瘤。以往,患者只能通过手术甚至截肢进行治疗。
Pexidartinib是一种口服集落刺激因子1受体抑制剂。
批准基于名为ENLIVEN的3期临床试验结果。
试验数据表明,接受治疗的患者中39%在25周治疗后获得缓解,而安慰剂组的客观缓解率为0%。
Myovant Sciences子宫肌瘤创新疗法
达到3期临床终点
近日,Myovant公司宣布其开发的Relugolix组合疗法在治疗子宫肌瘤的3期临床实验中达到主要终点和多项次要终点。
Relugolix是一种口服促性腺激素释放激素受体拮抗剂。
388名患有子宫肌瘤并且出现严重月经出血的患者在LIBERTY13期临床试验中,接受了relugolix组合疗法或安慰剂治疗。
试验数据显示,Relugolix显著缓解患者病情,73.4%的治疗组患者达到缓解标准,安慰剂组仅有18.9%的患者得到缓解。
新基卡波西肉瘤新药Pomalyst
获得突破性疗法认定
FDA授予新基治疗HIV阴性卡波西肉瘤患者的新药Pomalyst突破性疗法认定。
Pomalyst是一款口服沙利度胺类似物。
批准基于Pomalyst在22名患者中的1/2期临床试验。
试验数据显示,接受治疗的HIV患者ORR达到100%,CR达到14%。
首款不通过结合多巴胺受体治疗精神分裂症
的抗精神病药物获FDA突破疗法认定
近日,Sunovion和PsychoGenics公司治疗精神分裂症的在研新药SEP-363856获得美国FDA授予的突破性疗法认定,有望成为第一款不通过结合多巴胺D2受体来治疗精神分裂症的药物。
SEP-363856被认为有可能激活5-羟色胺1A受体以及痕量胺相关受体TAAR1(机制未明确)。
批准基于名为SEP361-201的随机、安慰剂对照、双盲注册研究。
试验数据显示,接受SEP-363856的患者,较安慰剂组阳性和阴性症状量表的总分有显著改善。
阿柏西普获批治疗所有阶段糖尿病视网膜病变
再生元宣布旗下眼科重磅药物Eylea(阿柏西普)获FDA批准用于治疗全阶段的糖尿病视网膜病变。
阿柏西普是一款VEGF抑制剂,2018年全球销量73.54亿美金。
批准基于名为PANORAMA的3期临床试验。
试验数据显示,接受Eylea治疗的患者视网膜病变改善比例(以DRSS量表评分提升两级为标准)达到65%(每16周注射一次)、80%(每8周注射一次),对照组的这一比例为15%。
辉瑞宣布旗下JAK抑制剂
在3期临床实验中取得积极顶线结果
辉瑞宣布其JAK1抑制剂abrocitinib在一项治疗中重度皮炎的3期临床试验中取得积极顶线结果。
Abrocitinib是一款口服JAK1抑制剂。
该临床实验为随机、双盲、安慰剂对照的3期临床试验。
治疗组中,患者达到主要疗效终点和关键次要终点的比例显著提高。
Unicure公布B型血友病基因疗法2期积极数据
Unicure公司公布了旗下B型血友病基因疗法AMT-061的2b期临床试验的积极数据。
AMT-061是一种联合AAV5载体和FIX-Padua变体的基因疗法,用于治疗中度及重度B型血友病。
AMT-061的2b期试验是一项开放标签、单剂量、单臂、多中心试验。目前3名患者接受了治疗。
单次使用AMT-061后6个月,接受治疗的3名患者凝血因子IX(FIX)活性持续升高,已有两名患者达到了正常水平。
Moderna在研mRNA流感疫苗在
1期实验中表现良好
Moderna发布其在研mRNA流感疫苗的1期实验数据。
Moderna此次公布数据的是H10N8流感疫苗mRNA-1440,及H7N9流感疫苗mRNA-1851。
两项1期临床实验中,201名/156名健康志愿者接受了疫苗或安慰剂注射。
试验数据显示,两款流感疫苗在1期实验中安全性良好,能够激发强力免疫反应。

❖拜耳宣布投资1.5亿元在加州伯克利建设一个细胞培养技术中心,以支持其不断扩张的生物制剂产品(特别是其预计21年底上线的肿瘤和心脏病项目)的生产开发,帮助更多患者群体。该中心将与Fluor和GE医疗合作。
❖复宏汉霖旗下利妥昔单抗注射液(汉利康)正式纳入上海医保,100mg/10ml/瓶的产品协议采购价定为1648元,个人定额自负标准为650元。
❖Vertex Pharmaceuticals和Kymera Therapeutics宣布将达成为期4年的研发协议,共同开发靶向多个靶点的小分子蛋白降解剂。Kymera可以获得7000万美金的预付款及潜在的超过10亿美元的里程碑付款和后续产品分成。
❖英国生物科技公司F-star宣布将修订与默克共同开发双特异性抗体肿瘤免疫治疗药物的合作协议。该协议于2017年达成,F-star通过修订协议获得了本授权予默克的四价双特异性抗体FS118的开发和商业化独家权利。
❖Forty Seven公司与阿斯利康旗下Acerta Pharma达成临床试验合作协议,将评估包括抗CD47单克隆抗体5F9、靶向药BTK抑制剂Calquence和利妥昔单抗的三联组合疗法在弥漫性大B细胞淋巴瘤中的治疗效果。
❖近日,BMS的日本合作方小野药品针对厚生省的O药不良反应通报回应,截至2018年11月7日,疑与Opdivo有因果关系的下垂体功能障碍为11例(黑色素瘤3例,非小细胞肺癌8例),其中死亡1例(非小细胞肺癌),具体原因尚不明确。这对胶质母细胞瘤的3期临床未能达到主要终点的O药更是雪上加霜。
❖雀巢宣布将以约101亿美金价格出售旗下皮肤健康业务,目前正与欧洲私募巨头EQT和阿布扎比投资局为首的财团进入独家裁判。
❖由于联邦贸易委员会的监管审查评估需要更多时间,罗氏43亿美金收购Sparks Therapeutics的计划第三次被延迟。
❖Blackstone近日以1.1万亿韩元(9.45亿美元)的价格从Anchor Equity Partners手中购入韩国药品分销商Geo-Young 46%的股份。
❖诺华CAR-T疗法Kymriah近日被纳入日本医保,用于治疗部分白血病或淋巴瘤,定价30.5万美金。
❖基因泰克与特异性免疫调节药物公司Parvus Therapeutics达成合作,共同研发、生产及商业化Parvus的免疫调节疗法Navacim。该疗法可以用于炎症性肠病、自身免疫肝病、乳糜泻的治疗。

































