
2017年7月12日,美国FDA肿瘤药物专家咨询委员会(ODAC)以10:0的投票结果,一致推荐批准由诺华和宾西法比亚大学开发的CAR-T疗法Tisagenlecleucel(CTL-019)上市。
CAR-T疗法是目前人类抗癌史上第一种可定向攻击癌细胞的疗法,是免疫疗法的一个分支。
CAR-T疗法的原理是从患者的血液中分离出人体免疫T细胞,再用基因工程技术给这些T细胞加入一个能识别肿瘤细胞,且同时激活T细胞的嵌合抗体。将这些细胞在体外扩增培养之后,在回输到病人体内,通过增强人体自身的免疫能力,来达到抗击癌细胞的目的。
这种疗法对急性白血病和非霍奇金淋巴瘤的治疗,有着显著的疗效。
CAR-T疗法被认为是目前最有前景的肿瘤治疗方式之一。但FDA委员为以10:0的比例全票通过,这在历史上实属罕见。
不过,这可能也更诺华的巧妙安排有关,投票是在两位年轻父亲的演讲后进行的,他们是这种疗法的受益者。
来自宾夕法尼亚的Tom Whitehead曾是一名白血病患儿的父亲。Tom Whitehead 12岁大的女儿Emily在五年前接受了CAR-T的实验治疗,她是第一个接受CAR-T疗法的儿童。Tom Whitehead表示:“我相信,一旦这种疗法获得批准,它将拯救世界各地数千计儿童的生命。”
国家癌症研究所的Malcolm A. Smith博士也在现场为诺华拉票,他认为:“这是癌症研究的重大进展,也许CAR-T将开创一个新的时代。”
FDA将在几个月后决定是否批准Tisagenlecleucel上市,就目前来看这种疗法成为全球首个获批上市的CRA-T疗法的可能性很大。
白血病在儿童和青年人中的发病率最高,诺华希望自己的产品能够被批准用于3-25岁、在接受常规治疗后没有反应的急性淋巴细胞白血病患者。这样的病例美国每年大约有600例。
这些患者不能通过常规的治疗方案得到病症的缓解,他们能够选择的治疗方案是有限的,且大部分方案的毒副作用都比CAR-T疗法强。可以说,这类癌症患者的生存机会非常渺小,这些人中,有1/4是15岁以下的儿童。
CAR-T疗法的日渐成熟,无疑是给这些人和患者家属带来了新的希望。在几个关键性测试中,CAR-T疗法的疗效要远远高于化疗、甚至一些新型的癌症药物。接受治疗的52名患者中,83%的人病症得到完全缓解。也就是说他们的癌症完全消失了。
但凡事都有两面性,CAR-T疗法并非是完美的。大部分接受治疗的患者都伴随严重的毒副反应,有11例患者治疗无效死亡。
CAR-T疗法的治疗费用大概需要几十万美元,并且患者只能使用一次。通常,患者需要服用一种或者多种药物。等到这些药物完全作用后,患者还要再改用其他药物。因此,这种疗法的治疗过程和副作用将伴随患者数年。
短期的副作用包括,发烧、幻视,更严重的可能发生免疫反应;长期副作用是未知的。如果患者进入癌症缓解期, 最终会完全治愈还是复发,这也是不清楚的。
FDA小组建议公司对接收治疗的患者进行为期15年的监测。
另外一点则是FDA顾问指出的。通常,患者在接受治疗前需要接受一系列检测,这个过程平均耗时16周。对于一些已经病入膏肓的患者来说,这么长的时间他可能等不起。诺华则表示,目前他们已经把时间缩短到3周。
CAR-T疗法的开发者其实不止诺华一家。在这场竞赛中,原本诺华的进度要落后于JUNO和Kite。但由于临床研究中先后出现5例脑水肿引起的患者死亡,JUNO的临床研究一度被FDA叫停。Kite制药的KTE-C19也在4月底出现1例患者死亡。
目前,Kite制药的CAR-T疗法同样已经进入FDA审查阶段,另一家公司 Therapeutics的产品也进入了最后的测试阶段。但鉴于FDA对CAR-T疗法安全性的谨慎,这两家公司要拿到最终的审批,可能还需要等待一段时间。
除CAR-T疗法外,一些生物技术公司和制药公司也在加紧关于治疗实体瘤和罕见病的基因疗法研究,其中一些产品已经在部分地区上市。比如2004年在中国上市的头颈部癌症连发,还有葛兰素史克去年在欧洲获批的干细胞疗法Strimvelis,UniQure在2012年获批的基因疗法Glybera。
不过,Strimvelis和Glybera的价格分别高达67万美元和100万美元,高昂的价格也许使得公司很难去开拓市场。
国内的CAR-T疗法研发实力也非常强,中国在在ClinicalTrials.gov登记的CAR-T相关临床研究数量仅次于美国。
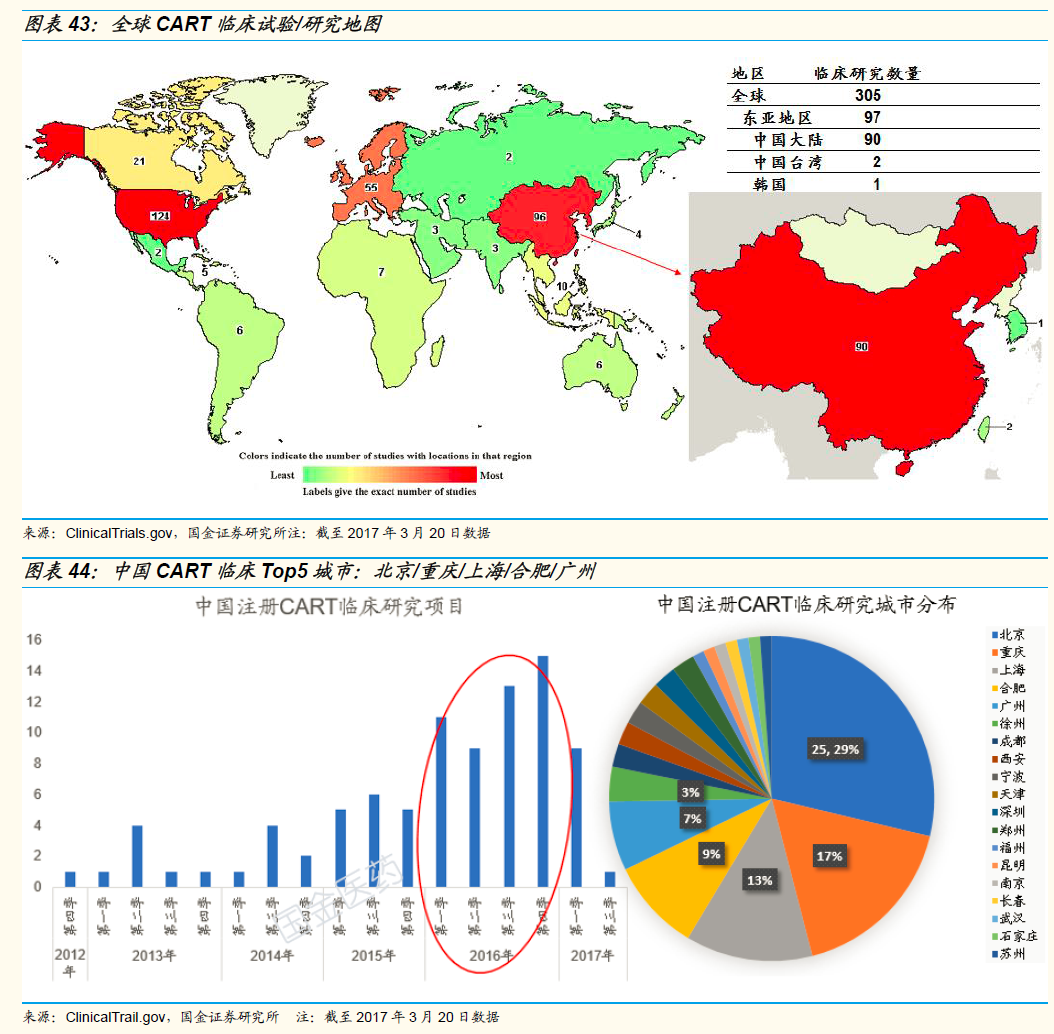
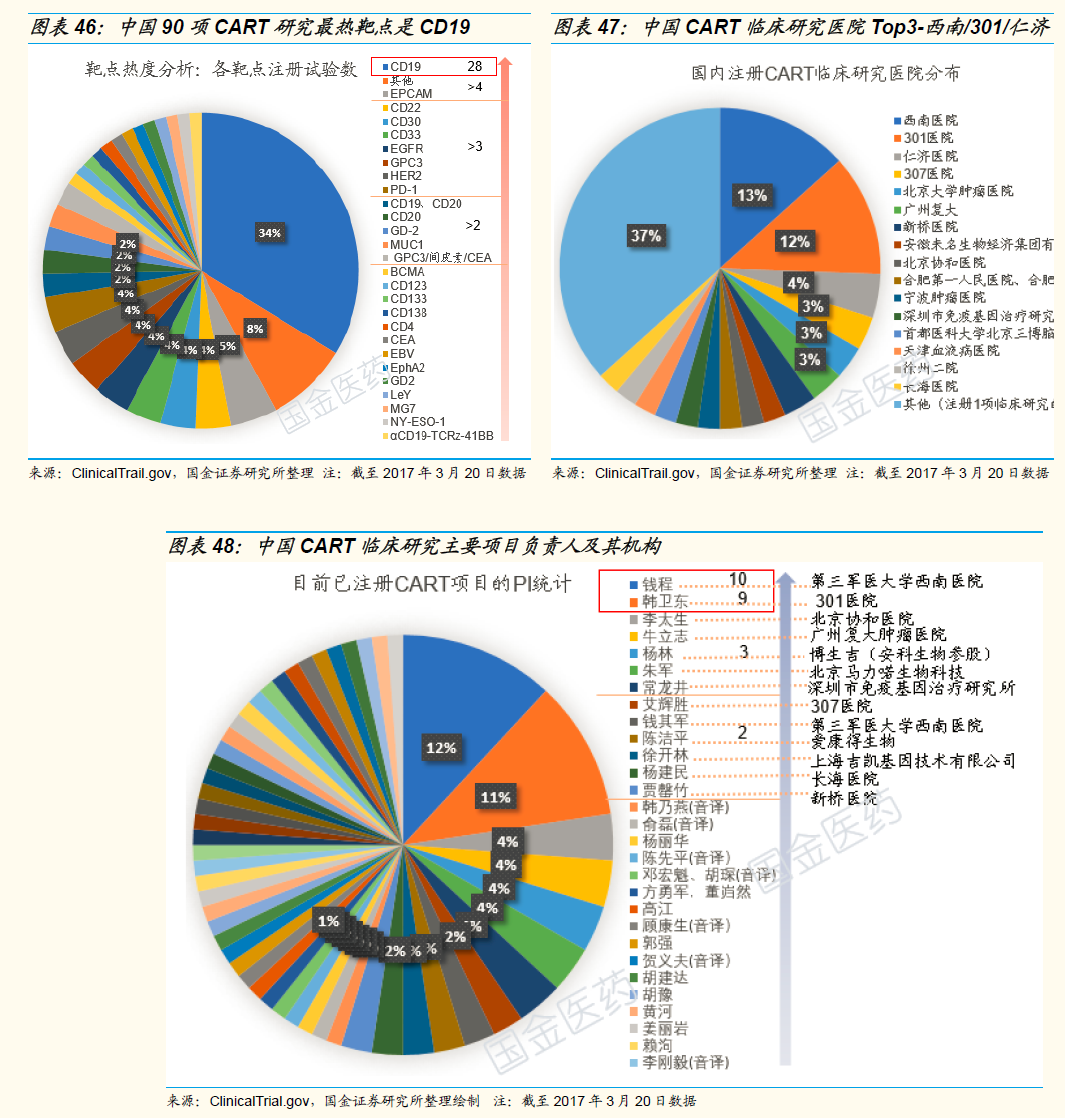
复星医药在今年1月斥巨资引进了Kite制药CAR-T产品中国市场开发权,另外解放军总医院,北京肿瘤医院,同济医院,源正细胞,爱康得,波睿达生物,上海吉凯基因,安科生物等大批医疗机构和公司都在此布局。
10:0这个比例,无疑也是给国内这些机构和公司打了一针强心剂。






























