10月9日,FDA拒绝了Alnylam Pharmaceuticals的siRNA药物Onpattro(patisiran)的补充新药应用(sNDA),用于治疗转甲状腺素蛋白介导(ATTR)淀粉样变性心肌病。
Alnylam公告表示,此次拒绝不影响patisiran用于治疗成人遗传性ATTR淀粉样变性多发性神经病(现有适应症)的商业可行性,但Alnylam将不再致力于在美国扩大patisiran的适应症。
这一结果与FDA外部顾问委员会的投票结果背道而驰。9月,外部顾问委员会以9:3的投票结果支持patisiran,认为此siRNA疗法的益处超过了其风险性。
监管机构在其完成回应函(CRL)中表示,Alnylam没有提供足够的证据证明patisiran在ATTR淀粉样变性心肌病治疗中的临床意义。与此同时,FDA并未指出patisiran的临床安全性、药品质量、生产工艺或研究行为存在任何问题。
不过,Alnylam在公告里表现出积极态度,称将继续致力于ATTR淀粉样变性病领域,并推动另一siRNA治疗药物vutrisiran(Amvuttra)用于治疗ATTR淀粉样变性心肌病(ATTR-CM)的研究。
转甲状腺素蛋白淀粉样变性(ATTR amyloidosis)是一种罕见疾病,主要引起多发性神经病变(ATTR-PN)和心肌病(ATTR-CM)。ATTR是由淀粉样蛋白的异常沉积物累积引起的,干扰器官的正常功能。这些蛋白质沉积物最常发生在心脏和周围神经系统中,并逐渐影响呼吸、肾脏、眼睛、胃肠道和中枢神经系统,导致心力衰竭、意识丧失、疼痛、运动障碍和死亡。
Patisiran是一种双链siRNA治疗剂,结合并靶向破坏编码转甲状腺素蛋白的mRNA分子。这一治疗机制将导致蛋白质总体水平较低,进而避免错误折叠的转甲状腺素蛋白在身体各个器官中出现病理性积累。
2018年8月,FDA首次批准Patisiran用于治疗成人遗传性ATTR淀粉样变性多发性神经病,成为全球获批的第一款RNAi药物,辐射全球患者约5万人。如果此次适应症扩展能够获批,Patisiran覆盖的患者还将包括影响了全球约20-30万人的wtATTR淀粉样变性。
而在ATTR-CM领域,Alnylam目前唯一的竞品为辉瑞的重磅小分子药物tafamidis(Vyndaqel/ Vyndamax)。2019年5月,FDA批准Vyndaqel和Vyndamax用于治疗ATTR-CM成人患者。这是全球首个、也是唯一经批准治疗ATTR-CM的药物(2020年中国获批上市)。
在辉瑞2023年第二季度财报中,Vyndaqel家族(Vyndaqel,Vyndamax,Vynmac)在全球范围内的经营同比增长了43%,达到7.82亿美元。同一时期,Onpattro的全球净产品收入为9100万美元。
二者可对比的一点在于向FDA提交的疗效证据。
FDA对tafamidis的批准基于其临床试验数据——辉瑞采用了一项纳入441名随机接受Vyndaqel或安慰剂的临床试验。平均30个月后,Vyndaqel组的存活率高于安慰剂组,证明可以帮助ATTR-CM患者延长寿命并减少因心血管疾病住院次数。
而Alnylam则是通过六分钟步行测试和生活质量调查(KCCQ-OS)表明,Onpattro相比于安慰剂有助于改善ATTR-CM淀粉样变性心肌病的身体机能和生活质量。
Alnylam首席执行官Yvonne Greenstreet在周一的电话会议上表示,用于支持Onpattro应用的第三阶段试验APOLLO-B是与FDA协商设计的。该试验达到了其主要终点,显示Onpattro服用者在六分钟步行测试中的统计学显著改善,并在24个月的随访中维持其临床益处。在KCCQ-OS患者报告调查中,该药物也显示出明显优于安慰剂,并且有改善心血管预后的趋势。
但是,FDA认为Onpattro的治疗效果根本没有临床意义。FDA在评估报告中写到,六分钟的步行测试也缺乏证实这一发现的依据,只有一部分的KCCQ-OS指标可以直接评估患者的身体机能。认为Onpattro的疗效很小的观点在9月的咨询委员会会议上也被提出,一位专家将其描述为“slight breeze”。同时,一些专家认为,Alnylam的药物不应作为替代tafamidis的同等选择。
公告表示,Alnylam打算继续为参加APOLLO-B第三阶段研究的OLE期患者和美国扩大接入协议(EAP)的ATTR-CM患者提供Onpattro。
与此同时,RNAi侯选药物vutrisiran的III期HELIOS-B研究也将继续,评估其对ATTR-CM患者30个月时全因死亡率和复发性心血管(CV)事件复合终点的疗效。候选管线ALN-TTRsc04也将适应症对准ATTR-CM,利用IKARIA技术,每年一次给药剂量可能使TTR(转甲状腺素蛋白)降低超过90%。
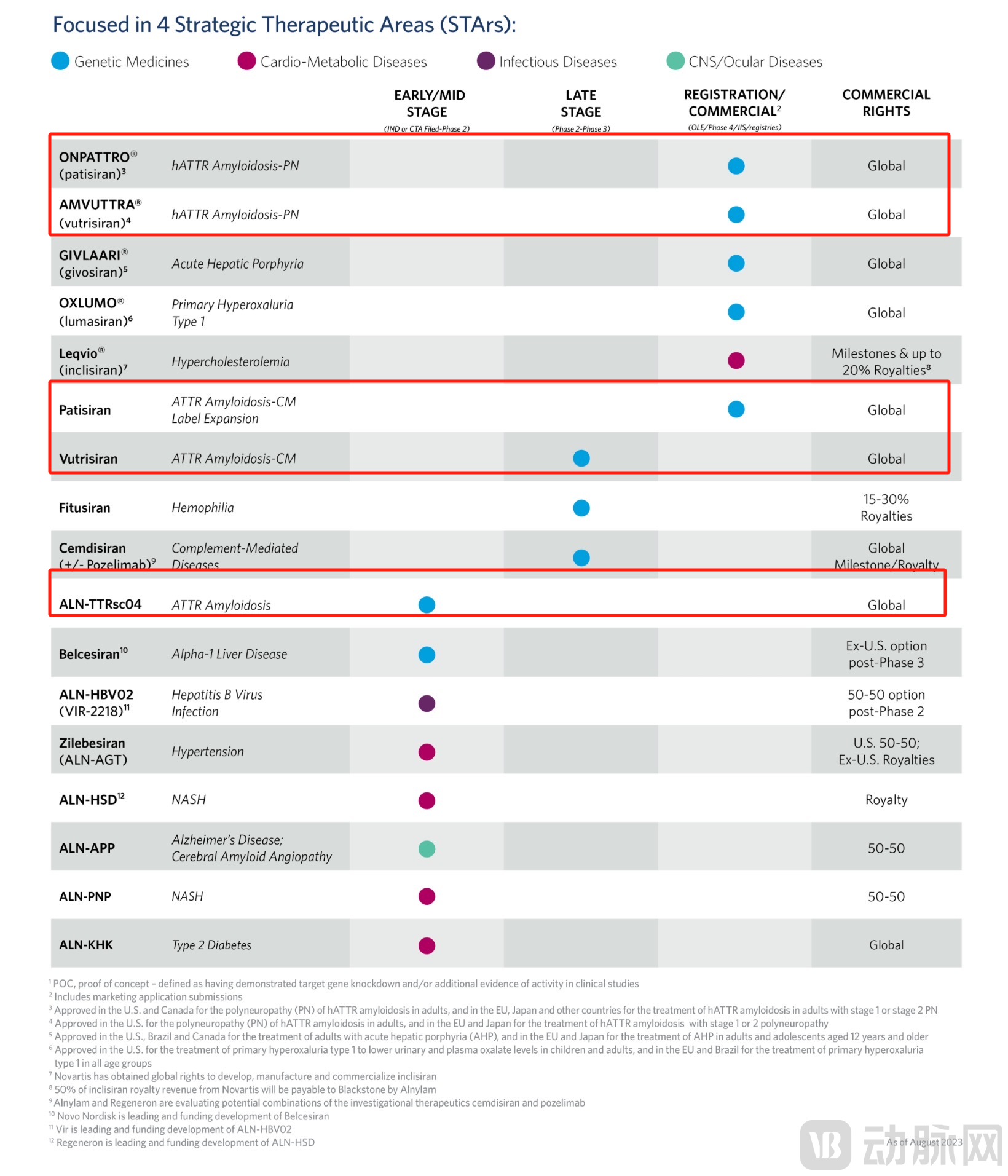
Alnylam管线布局(红框为ATTR赛道)
要看懂Alnylam“弃卒保车”的战略性调整,首先要先回到Alnylam的“明星企业”光环上。2022年12月23日,Alnylam股价达到峰值,来到237.90美元的最高点。
作为全球RNAi头部企业,Alnylam在其21年的发展中契合了RNAi技术的发展历程——在本世纪最初10年中曾被寄予厚望,陷入困境后又一鸣惊人,最终进入稳步变现期。
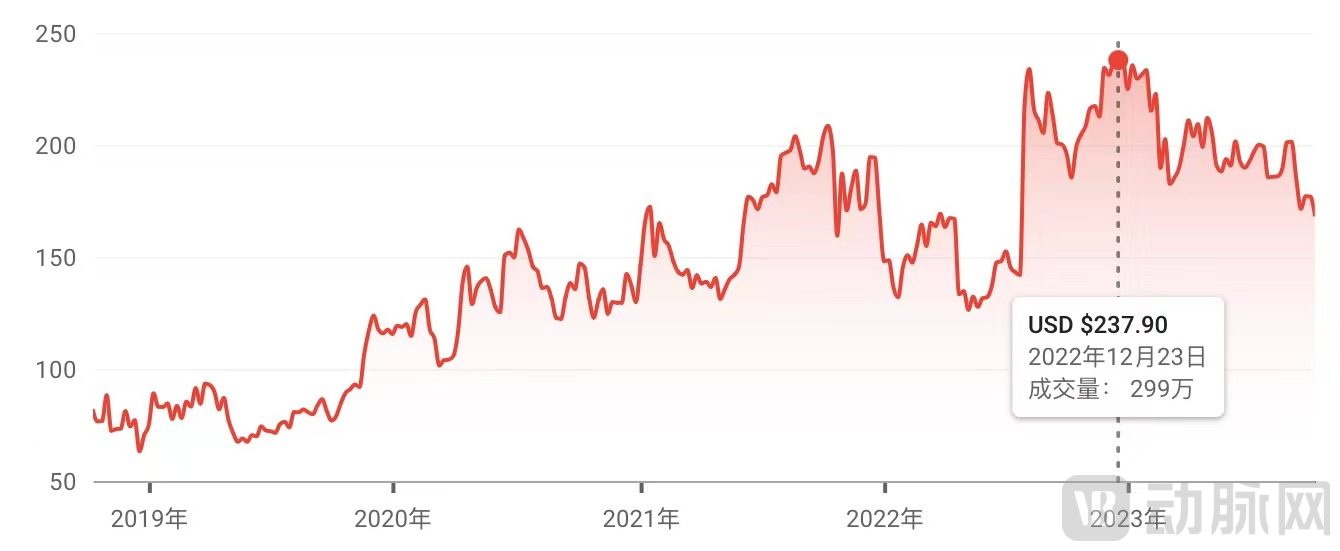
Alnylam股票(图源:Google Finance)
Alnylam的“一鸣惊人”在于引领GalNAc(乙酰半乳糖胺转移酶)的第三代递送技术潮流。在RNAi技术研发上,递送技术一直是急需攻克的重难点。第二代载体(脂质纳米颗粒)在很长的一段时间中都是siRNA递送的核心方法,Alnylam在最初的十几年的时间也一直在优化LNP递送平台。
本次适应症拓展的主角、全球首款RNAi药物patisiran就是Alnylam早期药物管线,也是其在第二代LNP递送平台上推出的一款产品。
在Onpattro获批之前,Alnylam就已经在深度布局围绕着GalNAc的新递送技术。以GalNAc为基础的第三代递送方案,凭借低免疫原性、低细胞毒性和高靶向性,解决了以往二代LNP递送平台的部分问题,让siRNA能够大展拳脚。
Alnylam引领的GalNAc潮流给他们带来了巨大的先发优势。这也是为何多款上市的siRNA产品都与Alnylam存在关联。例如Alnylam用于治疗急性肝卟啉症(AHP)的Givlaari、治疗原发性高草尿酸症1型的Oxlumo、与诺华共同开发的靶向降脂药物Leqvio,也都采用了新的GalNAc递送技术。
借助罕见病药物的研发和成功上市迅速成为siRNA龙头后,Alnylam继续扩展RNAi管线资产,布局在遗传药物、心脏代谢疾病、传染病、中枢神经系统及眼部疾病。利用罕见病药物研发得到的技术积累与洞见,Alnylam正在攻破乙肝、非酒精性脂肪性肝炎等常见病——“我们的目标是每年产生2-4个新的IND(研究性新药)申请”。
回到Alnylam起家的罕见病ATTR布局上,首款药物patisiran(Onpattro)和第二款药物vutrisiran(Amvuttra)先后上市,均已在全球实现商业化。2023年第二季度,Onpattro和Amvuttra全球净产品收入分别为9100万美元和1.32亿美元,同比增长率为46%。其中美国市场的总增长率连续一年超过70%。
二者区别不仅在于递送系统的更新,还在于给药方式的不同上。Onpattro为每3周1次的静脉注射;Amvuttra则为每3月1次的皮下注射,具有每6月给药1次的潜力。而此次公告中提及的ALN-TTRsc04管线,则有望达到每年1次的给药频率。
到这里,Alnylam“两手抓”的ATTR战略已然明了——以Onpattro立足、Amvuttra抢占更大市场份额,占据巨大的ATTR市场。下一步,一方面通过对2款上市药物扩展适应症以继续提升市场规模,另一方面继续药物迭代,巩固Alnylam在ATTR的市场规模优势。
Alnylam将其称为“bridging strategy”。






























